
| 选项 | 实验 | 现象 | 离子方程式 |
| A | 向氯化铝溶液中滴加过量氨水 | 有白色沉淀产生 | Al3++3OH-=Al(OH)3↓ |
| B | 向FeBr2溶液中通入少量氯气 | 溶液由浅绿色变成黄色 | 2Fe2++Cl2=2Fe3++2Cl- |
| C | 向稀硝酸中加入单质Fe粉 | 有气泡生成 | Fe+6H+=3Fe3++3H2↑ |
| D | 向Na2CO3溶液中滴加酚酞试剂 | 溶液由无色变为红色 | CO32-+H2O=H2CO3+2OH- |
| A. | A | B. | B | C. | C | D. | D |
分析 A.一水合氨为弱电解质,离子方程式中不能拆开,应该保留分子式;
B.亚铁离子的还原性大于溴离子,氯气少量,浅绿色亚铁离子优先被氧化成黄色的铁离子;
C.铁与稀硝酸反应生成NO气体,不会生成氢气;
D.碳酸根离子的水解分步进行,主要以第一步为主,水解的离子方程式只写出第一步即可.
解答 解:A.向氯化铝溶液中滴加过量氨水可以获得氢氧化铝白色沉淀,一水合氨不能拆开,正确的离子方程式为:Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故A错误;
B.向FeBr2溶液中通入少量氯气,亚铁离子优先被氧化,溶液由浅绿色变成黄色,反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,故B正确;
C.铁与稀硝酸反应生成NO气体,不会产生氢气,如:铁过量时,稀硝酸与过量的铁粉反应生成硝酸亚铁和一氧化氮和水,离子方程式为:3Fe+8H++2N03-═3Fe2++2NO↑+4H2O,故C错误;
D.碳酸根离子水解主要以第一步为主,正确的离子方程式为:CO32-+H2O=HCO3-+OH-,故D错误;
故选B.
点评 本题考查了离子方程式的正误判断,为高考中的高频题,属于中等难度的试题,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等;本题中还要注意反应现象是否正确.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
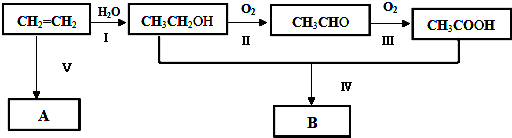
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应涉及到离子键和共价键的断裂与形成 | |
| B. | 该反应中,化学能只转变为热能 | |
| C. | 断开1molH-H键和1molCl-Cl键所吸收的总能量,小于形成1molH-Cl键所放出的能量 | |
| D. | 反应物所具有的总能量高于产物所具有的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
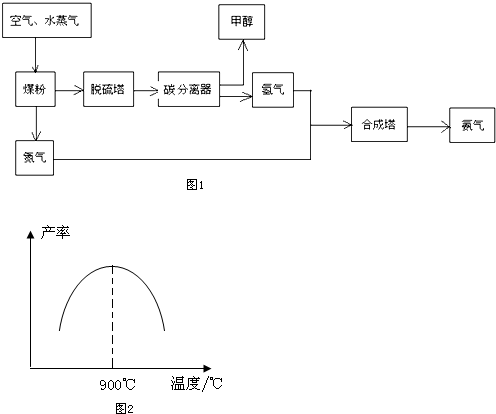
| 物质 | H2 | CO | C H3OH |
| 浓度/(mol•L-1) | 0.20 | o.10 | o.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
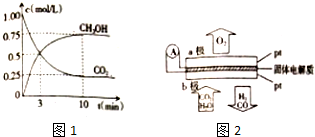
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳与赤热的炭反应生成一氧化碳 | |
| B. | 葡萄糖在人体内氧化分解 | |
| C. | 锌粒与稀H2SO4反应制取H2 | |
| D. | Ba(OH)2•8H2O与NH4Cl反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ①②④ | C. | ①④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com