
| A. | $\frac{3{V}_{1}-{V}_{2}}{{V}_{1}+{V}_{2}}$ | |
| B. | $\frac{({V}_{1}+{V}_{2})×1{0}^{-14}}{{V}_{2}-3{V}_{1}}$ | |
| C. | $\frac{({V}_{1}{P}_{1}+{V}_{2}{P}_{2})×1{0}^{-14}}{({V}_{2}-3{V}_{1}){P}_{3}}$ | |
| D. | $\frac{({V}_{1}{P}_{1}+{V}_{2}{P}_{2})×1{0}^{-14}}{(3{V}_{1}-{V}_{2}){P}_{3}}$ |
分析 将V1 mL 1.5mol/L H2SO4溶液与V2 mL 1mol/L NaOH溶液混合,所得混合液中氢氧化钠的物质的量=V2×0.001×1mol/L-V1×0.001×1.5mol/L×2=0.001(V2-3V1)mol,测得混合液的密度为ρ3 g/mL,溶液的质量V1ρ1+ρ2V2,结合Kw=c(H+)•c(OH-)来计算即可.
解答 解:将V1 mL 1.5mol/L H2SO4溶液与V2 mL 1mol/L NaOH溶液混合,所得混合液中氢氧化钠的物质的量=V2×0.001×1mol/L-V1×0.001×1.5mol/L×2=0.001(V2-3V1)mol,测得混合液的密度为ρ3 g/mL,溶液的质量V1ρ1+ρ2V2,所以混合后溶液的体积=$\frac{{V}_{1}{ρ}_{1}+{V}_{2}{ρ}_{2}}{{ρ}_{3}}$mL,所以氢氧根离子浓度=$\frac{{0.001(V}_{2}-3{V}_{1})}{\frac{{V}_{1}{ρ}_{1}+{V}_{2}{ρ}_{2}}{{ρ}_{3}}×0.001}$mol/L=$\frac{{{ρ}_{3}(V}_{2}-3{V}_{1})}{{V}_{1}{ρ}_{1}+{V}_{2}{ρ}_{2}}$mol/L,根据Kw=c(H+)•c(OH-),得到混合溶液中c(H+)为$\frac{({V}_{1}{ρ}_{1}+{V}_{2}{ρ}_{2})×1{0}^{-14}}{({V}_{2}-3{V}_{1})•{ρ}_{3}}$.
故选C.
点评 本题考查学生溶液中离子浓度的计算,注意水的离子积常数的应用是关键,难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
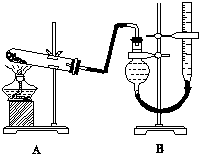 某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ④ | 1.2g | 无其他物质 | |
| ⑤[ | 1.2g | CuO 0.5g | |
| ⑥ | 1.2g | MnO2 0.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10 mol | B. | 11 mol | C. | 12 mol | D. | 13 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠在空气和氯气中燃烧,火焰皆呈黄色,但生成固体颜色不同 | |
| B. | 新制饱和氯水和浓硝酸光照下会有气体产生,其成分中有氧气 | |
| C. | 次氯酸和过氧化钠都能使品红溶液褪色,其原理是不相同的 | |
| D. | Mg在CO2中燃烧生成MgO和C,在该反应条件下,Mg的还原性强于C的还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| 选项 | a中的物质 | b中的物质 | c中的物质 | d中的物质 | d中的物质 |
| A | 浓硫酸 | 铜片 | 品红溶液 | 酸性高锰酸钾溶液 | c,d中溶液颜色均褪色,依次体现SO2漂白性和还原性 |
| B | 浓硫酸 | 蔗糖 | 紫色石蕊溶液 | NaOH溶液 | c中溶液变红色,不能判断是SO2的作用 |
| C | 稀硝酸 | Cu | 收集NO2 | H2O | d中反应每消耗3mol氧化剂,转移2mol电子 |
| D | 浓氨水 | 碱石灰 | 收集NH3 | 稀H2SO4 | d中反应产物可作肥料 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池工作时,锌失去电子 | |
| B. | 电池正极的电极反应式为:2MnO2+2H2O+2e-═2MnOOH+2OH- | |
| C. | 电池工作时,电子由正极通过外电路流向负极 | |
| D. | 外电路中每通过0.2mol 电子,锌的质量理论上减少6.5g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com