
| A. | 在0.1mol•L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| B. | 在0.1mol•L-1Na2CO3溶液中:c(OH-)+c(H+)=c(HCO3-)+2c(H2CO3) | |
| C. | 向0.2mol•L-1NaHCO3溶液中加入等体积0.1mol•L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | 常温下,CH2COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1mol•L-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-) |
分析 A.碳酸氢钠溶液中,碳酸氢根离子的水解程度大于其电离程度,则溶液中c(H2CO3)>c(CO32-);
B.根据碳酸钠溶液中的质子守恒判断;
C.反应后的溶质为等物质的量的碳酸钠、碳酸氢钠,碳酸根离子的水解程度大于碳酸氢根离子,则溶液中碳酸氢根离子浓度大于碳酸根离子;
D.CH3COONa和CH3COOH混合溶液的pH=7,显示中性,据电荷守恒、溶液组成进行分析.
解答 解:A.碳酸氢钠溶液中,碳酸氢根离子的电离程度小于其水解程度,溶液显示碱性,则:c(H2CO3)>c(CO32-),溶液中正确的粒子难度大小为:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-),故A错误;
B.根据碳酸钠溶液中的质子守恒可得:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3),故B错误;
C.向0.2mol•L-1NaHCO3溶液中加入等体积0.1mol•L-1NaOH溶液,反应后溶质为等浓度的NaHCO3、Na2CO3,CO32-的水解程度大于HCO3-,则:c(HCO3-)>c(CO32-),溶液中正确的离子浓度关系为:c(HCO3-)>c(CO32-)>c(OH-)>c(H+),故C错误;
D.CH3COONa和CH3COOH混合溶液的pH=7,则c(H+)=c(OH-),根据电荷守恒可得:c(Na+)=c(CH3COO-)=O.1mol/l,溶液中离子浓度大小为:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-),故D正确;
故选D.
点评 本题考查离子浓度大小比较、盐的水解原理及其应用等知识,题目难度中等,明确电荷守恒、物料守恒以及质子守恒的应用为解答关键,注意掌握盐的水解原理.


 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案科目:高中化学 来源: 题型:解答题
 天然气含有硫化氢气体,回收并综合利用硫化氢有重要的经济价值和环境保护意义.如硫化氢可经过一系列反应制得硫酸:
天然气含有硫化氢气体,回收并综合利用硫化氢有重要的经济价值和环境保护意义.如硫化氢可经过一系列反应制得硫酸:时间 物质 | 0min | 20min | 60min | 90min | 120min |
| H2S | 0.006 | 0.005 | |||
| H2 | 0 | 0.002 | 0.004 | ||
| S2 | 0 | 0.002 | 0.0025 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
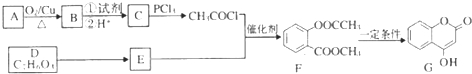
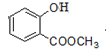
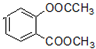 +3NaOH→CH3COONa+CH3OH+
+3NaOH→CH3COONa+CH3OH+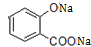 +H2O.
+H2O.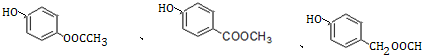 (写出其中一种的结构简式).
(写出其中一种的结构简式).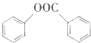 )是一种重要的有机合成中间体,试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任用)
)是一种重要的有机合成中间体,试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任用)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 时间/s | 0 | 5 | 10 | 15 |
| c(NO2)mol/L | 4.00 | 2.52 | 2.00 | c3 |
| c(O2)mol/L | 1.00 | c1 | c2 | 0.50 |
| A. | 5s内O2的反应速率为0.074mol/L•s) | |
| B. | T1℃时平衡常数为0.125,平衡时NO2和O2的转化率均为50% | |
| C. | T1℃时平衡常数为K1,T2℃时平衡常数为K2,若T1>T2,则K1<K2 | |
| D. | 其它条件不变,将容器的体积的压缩到原来的一半,则重新达到平衡时c(N2O3)<2mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
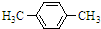 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$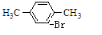 +HBr.
+HBr.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用四氯化碳可以萃取乙酸水溶液中的乙酸 | |
| B. | 丁烷有两种同分异构体 | |
| C. | 乙烯可以与氢气发生加成反应,也可发生自身加聚反应生成聚乙烯 | |
| D. | 纤维素、淀粉和蛋白质都是高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
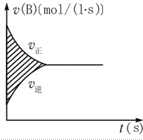
| A. | A浓度的减小量 | B. | B浓度的减小量 | ||
| C. | C物质的量的增加量 | D. | B物质的量的减少量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
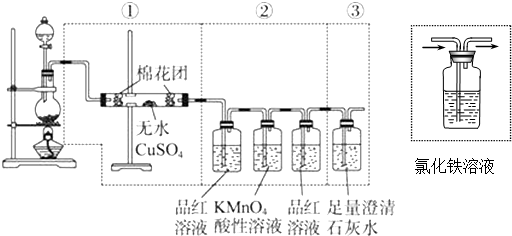
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com