
分析 (1)根据燃烧热的概念;
(2)根据氢气物质的量以及燃烧热、丙烷物质的量以及燃烧热,列式求出混合气体完全燃烧释放的热量;
(3)根据H2和C3H8的燃烧热,然后设出H2的物质的量,利用方程式组来解.
解答 解:(1)因燃烧热在某一温度和压强下lmol某物质B完全燃烧生成稳定化合物时所释放出的热量,所以H2的燃烧热为285.8kJ•mol-1,C3H8的燃烧热为2220kJ•mol-1,
故答案为:285.8kJ•mol-1;2220kJ•mol-1;
(2)1mol H2和2mol C3H8组成的混合气体完全燃烧释放的热量为1mol×285.8kJ•mol-1+2mol×2220kJ•mol-1=4725.8kJ,故答案为:4725.8kJ;
(3)设混合气中H2的物质的量为x,则C3H8的物质的量为5mol-x.根据题意,列方程为:
285.8kJ/mol×x+2220.0kJ/mol×(5mol-x)=3847kJ
解得 x=3.75 mol;C3H8的物质的量为5mol-3.75mol=1.25mol.
所以混合气体中H2与C3H8的体积比即物质的量之比为3:1,故答案为:3:1.
点评 本题主要考查了热化学方程式的计算,注意知识的迁移应用是关键,难度不大.


科目:高中化学 来源: 题型:解答题
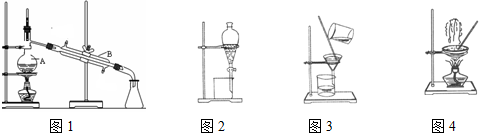
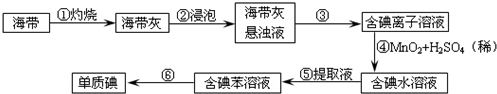
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
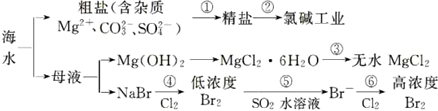
| A. | 过程①的提纯只有物理过程,过程②通过氧化还原反应可产生两种单质 | |
| B. | 在过程③中将MgCl2•6H2O真接灼烧即可制得纯净无水MgCl2 | |
| C. | 过程⑥所得的高浓度溴水只需分液即可获得液溴 | |
| D. | 过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀间题 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
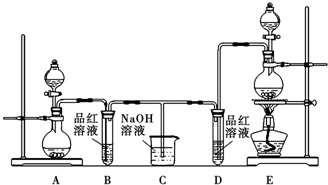
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .A、C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等.
.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等. ,C的氢化物与B的氢化物的稳定性强弱顺序为HF>H2S(填化学式).
,C的氢化物与B的氢化物的稳定性强弱顺序为HF>H2S(填化学式). .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 维生素A的一个分子中有五个双键 | |
| B. | 维生素A是一种烯烃 | |
| C. | 维生素A能使溴水褪色,能被酸性KMnO4氧化 | |
| D. | 维生素A的一个分子中有30个氢原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作与现象 | 解释或结论 |
| A | 过量的铁粉中加入稀硝酸中,充分反应后,滴入KSCN溶液,溶液呈红色 | 稀硝酸将Fe氧化为Fe3+ |
| B | AgI固体中滴入KCl溶液,沉淀由黄色变为白色 | AgI比AgCl难溶 |
| C | 铝箔插入稀硝酸中,无现象 | 铝箔表面被硝酸氧化,形成致密的氧化膜 |
| D | 苯酚溶液中滴加溴水,出现白色沉淀 | 苯酚易发生取代反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com