
| A、常温常压下,3.0 g乙烷中含有的碳氢键数为0.7NA |
| B、将0.2 mol FeCl3水解制成胶体,所得胶体粒子数为 0.2NA |
| C、常温常压下,28 g的 C2H4和C3H6混合气体含有的原子数为 6NA |
| D、标准状况下,由Na2O2制得11.2 L O2,反应转移的电子数为0.5NA |


科目:高中化学 来源: 题型:
| A、Cu原子的激发态简化电子排布式为[Ar]3d104s1 |
| B、Fe原子的外围电子排布式为4s2 |
C、丙烷分子的比例模型: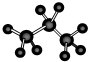 |
D、CH4Si的结构式: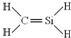 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2的摩尔质量为44g |
| B、5.4gH2O中有1.806×1023个原子 |
| C、CH4的相对分子质量为16g |
| D、2mol Cl2和2mol CO2所含分子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、体积:④<①<②<③ |
| B、密度:①<④<③<② |
| C、质量:④<①<③<② |
| D、氢原子数:②<④<③<① |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
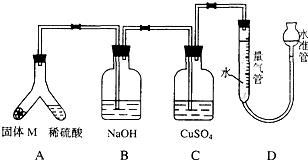 某课外兴趣小组为了探究铁与硫在隔绝空气的条件下反应所得固体M的成分,设计了如图装置.倾斜A使稀硫酸(足量)与固体M充分反应,待反应停止后,B装置增重,C装置中溶液无变化,反应后进入量气管气体的体积为VmL(已折算成标准状况)
某课外兴趣小组为了探究铁与硫在隔绝空气的条件下反应所得固体M的成分,设计了如图装置.倾斜A使稀硫酸(足量)与固体M充分反应,待反应停止后,B装置增重,C装置中溶液无变化,反应后进入量气管气体的体积为VmL(已折算成标准状况)查看答案和解析>>
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:
 甲、乙探究小组同学对铁及其化合物的性质进行了探究,试回答下列问题:
甲、乙探究小组同学对铁及其化合物的性质进行了探究,试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com