
| A. | 烧碱、纯碱、熟石灰均属于碱 | |
| B. | 稀豆浆、FeCl3溶液、牛奶均属于胶体 | |
| C. | HCl、BaSO4、NH3•H2O均属于电解质 | |
| D. | MgO、CuO、Na2O2均属于碱性氧化物 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:实验题
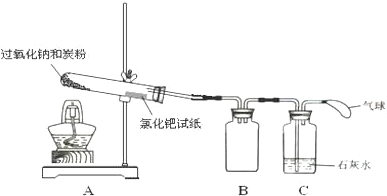
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当$\frac{a}{b}$>2时,发生的离子反应为:CO32-+H+═HCO3-,HCO3-+H+═CO2↑+H2O | |
| B. | 当0<$\frac{a}{b}$<1时,发生的离子反应为:CO32-+H+═HCO3- | |
| C. | 当2a=3b时,发生的离子反应为:2CO32-+3H+═HCO3-+CO2↑+H2O | |
| D. | 当1<$\frac{a}{b}$<2时,溶液中n(HCO3-)为(2a-b)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
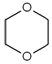 ).
).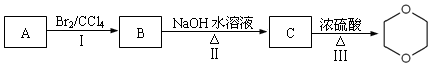
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 再滴加AgNO3溶液,观察是否有AgI沉淀产生 | |
| B. | 加入CCl4振荡后,观察下层液体颜色 | |
| C. | 加入CCl4振荡后,取上层清液,滴加KSCN溶液,观察是否出现红色 | |
| D. | 加入CCl4振荡后,取上层清液,滴加入AgNO3溶液,观察是否有AgCl沉淀产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 试剂X选用稀硝酸最合适 | |
| B. | 滤渣Y的主要成分为Fe2O3 | |
| C. | 反应I 中发生的反应之一为Al2O3+2OH-=2AlO2-+H2O | |
| D. | 减压蒸发结晶不能改为常压蒸发结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ②③④⑥ | C. | ②④⑤ | D. | ③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
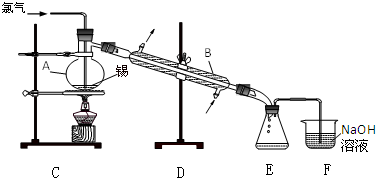
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水晶能溶于水生成H2SiO3 | |
| B. | SiO2是酸性氧化物,不能与任何酸反应 | |
| C. | SiO2既能溶于NaOH溶液,又能溶于HF,因此属于两性氧化物 | |
| D. | SiO2对应的H2SiO3是一种弱酸,酸性比碳酸还弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com