
| ||
| ||
| ||
| ||


 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
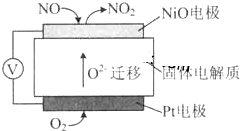
| A��NiO�缫�Ǹõ�ص����� |
| B��Pt�缫������pH���� |
| C��NiO�缫�ĵ缫��Ӧʽ��NO-2e-+O2-�TNO2 |
| D������������O2-�������ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ͨ�������Һ�У�NH3+H+=NH4+ | ||||
| B��̼���Ⱶ��Һ�м����������������Һ��Ba2++HCO3-+OH-=BaCO3��+H2O | ||||
| C����������������Һ�м���������⣺2Fe2++2H++H2O2=2Fe3++2H2O | ||||
D���ö��Ե缫�������ͭ��Һ��Cu2++2H+
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��K+��H+��NO3-��Cl- |
| B��Cu2+��Cl-��OH-��SO42- |
| C��H+��Na+��HCO3-��Cl- |
| D��Ca2+��Cl-��K+��CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ϡ H2SO4�����۷�Ӧ��2Fe+6H+=2Fe3++3H2�� | ||
| B��Cl2��ˮ�ķ�Ӧ��Cl2+H2O=2 H++Cl-+ClO- | ||
C����NH4��2SO4��Һ�м���Ba��OH��2��Ba2++SO
| ||
| D��FeCl2��Һ��Cl2��Ӧ��2Fe2++Cl2=2Fe3++2Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ʵ��������480mL 0.1mol?L-1NaOH��Һ���ش���������
ʵ��������480mL 0.1mol?L-1NaOH��Һ���ش����������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ܷ�ӦΪMg+H2O2�TMg��OH��2 |
| B�����������ĵ缫��ӦΪH2O2+2H++2e-�T2H2O |
| C������ʱ��������Χ��ˮ��pH��С |
| D����ع���ʱ����Һ�е�H+���ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��9�� | B��10�� |
| C��12�� | D��15�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com