
 ��
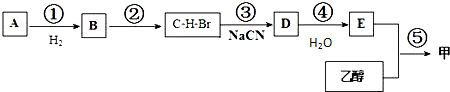
������ A����Է�������Ϊ106��5.3gA��ȫȼ��ʱ������CO2��2.7gH2O��A�Ͷ�����̼��ˮ�����ʵ���֮��=$\frac{5.3g}{106g/mol}$��$\frac{15.4g}{44g/mol}$��$\frac{2.7g}{18g/mol}$=0.05��0.35��0.15=1��7��3�����Ը÷����к���7��ԭ�Ӻ�6����ԭ�ӣ��������Է�������֪��������һ����ԭ�ӣ�����A�ķ���ʽΪC7H6O��A�ܷ���������Ӧ������A�к���ȩ�����䲻���Ͷ�=$\frac{2��7+2-6}{2}$=5��A�к��б�������A��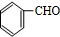 ������ȩ�����������ӳɷ�Ӧ����B��B��Ӧ����
������ȩ�����������ӳɷ�Ӧ����B��B��Ӧ����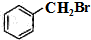 ����B�DZ��״������״����廯�ⷢ��ȡ����Ӧ����
����B�DZ��״������״����廯�ⷢ��ȡ����Ӧ���� ��
�� ���軯�Ʒ�Ӧ����D����������Ϣ֪��D�Ľṹ��ʽΪ��
���軯�Ʒ�Ӧ����D����������Ϣ֪��D�Ľṹ��ʽΪ�� ��
�� ��Ӧ����E��E�ܺ��Ҵ���Ӧ����������E�����ᣬ��������Ϣ֪��E��
��Ӧ����E��E�ܺ��Ҵ���Ӧ����������E�����ᣬ��������Ϣ֪��E�� ������
������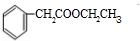 ��
��
��� �⣺A����Է�������Ϊ106��5.3gA��ȫȼ��ʱ������CO2��2.7gH2O��A�Ͷ�����̼��ˮ�����ʵ���֮��=$\frac{5.3g}{106g/mol}$��$\frac{15.4g}{44g/mol}$��$\frac{2.7g}{18g/mol}$=0.05��0.35��0.15=1��7��3�����Ը÷����к���7��ԭ�Ӻ�6����ԭ�ӣ��������Է�������֪��������һ����ԭ�ӣ�����A�ķ���ʽΪC7H6O��A�ܷ���������Ӧ������A�к���ȩ�����䲻���Ͷ�=$\frac{2��7+2-6}{2}$=5��A�к��б�������A�� ������ȩ�����������ӳɷ�Ӧ����B��B��Ӧ����
������ȩ�����������ӳɷ�Ӧ����B��B��Ӧ���� ����B�DZ��״������״����廯�ⷢ��ȡ����Ӧ����
����B�DZ��״������״����廯�ⷢ��ȡ����Ӧ���� ��
�� ���軯�Ʒ�Ӧ����D����������Ϣ֪��D�Ľṹ��ʽΪ��
���軯�Ʒ�Ӧ����D����������Ϣ֪��D�Ľṹ��ʽΪ�� ��
�� ��Ӧ����E��E�ܺ��Ҵ���Ӧ����������E�����ᣬ��������Ϣ֪��E��
��Ӧ����E��E�ܺ��Ҵ���Ӧ����������E�����ᣬ��������Ϣ֪��E�� ������
������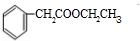 ��
��
��1��A�DZ���ȩ������ȩ�ķ���ʽC7H6O���䱽���Ϻ���3����ԭ�ӣ������䱽����һ�ȴ�����3�֣��ʴ�Ϊ��C7H6O��3��
��2���屽����ȡ����Ӧ����D�����Է�Ӧ�۵ķ�Ӧ������ ȡ����Ӧ���ʴ�Ϊ��ȡ����Ӧ��
��3����������Ҵ���Ũ���������������������·���������Ӧ���ɱ�������������ѧ����ʽ ��
��
�ʴ�Ϊ�� ��
��
��4��5.3g A���ʵ���Ϊ0.05mol����������������������ͭ����Һ�У����ȳ�ַ�Ӧ����-CHO��Cu2O����֪����Cu2O������Ϊ0.05mol��144g/mol=7.2g���ʴ�Ϊ��7.2��
���� ���⿼���л����ƶϣ����ؿ���ѧ�������ƶ���������ȷ�ж�A�Ľṹ��ʽ�ǽⱾ��ؼ������ݷ�Ӧ������������Ϣ�����ƶϣ�֪��������Ӧ���ͼ��л���ṹ����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
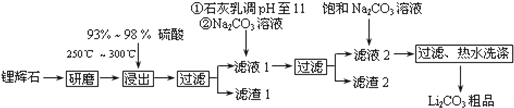
| T/�� | 20 | 40 | 60 | 80 |
| S��Li2CO3��/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S��Li2SO4��/g | 34.2 | 32.8 | 31.9 | 30.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ơ����Ż�Ӧ������ˮ���� | |
| B�� | ȼ�ŵľƾ��ƴ�ʧ��Ӧ������ˮ���� | |
| C�� | ����ʳ����Һʱ������Һ�ηɽ�����Ӧ������ˮ��ȴ | |
| D�� | Ƥ����մ������Ũ��������ô���ˮ��ϴ����Ϳ��3%��5%������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HF��HI | B�� | CCl4��CF4 | C�� | SiO2��CO2 | D�� | NaCl��KCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol�״��к���C-H������ĿΪ4NA | |
| B�� | ��״���£�22.4L CCl4���и�NA��CCl4���� | |
| C�� | 2.3g�ױ��ͱ�������C3H8O3���Ļ�����У�����ԭ����ĿΪ0.2NA | |
| D�� | ��״���£�2.24 L�������к����ۼ���ĿΪ0.7NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
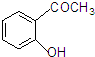 �ң�
�ң�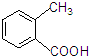 ����
����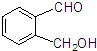
| �Լ� | ���� | |
| �� | Ũ��ˮ��FeCl3��Һ | ��ɫ��������Һ����ɫ |
| �� | ̼��������Һ | �������� |
| �� | ������Һ��Cu��OH��2 | ������ש��ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
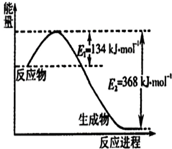 ̼�ǵ����Ϻ����ḻ��Ԫ�أ�����������о�������Ҫ���壮
̼�ǵ����Ϻ����ḻ��Ԫ�أ�����������о�������Ҫ���壮�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com