
【题目】某重要有机合成中间体X的结构如图所示,有关该物质的说法正确的是

A. X分子中所有碳原子一定共面
B. X可以使溴水、酸性KMnO4褪色,且原理不相同
C. 标况下1 molX分别和足量Na和NaHCO3反应,生成气体体积相同
D. X与庚二酸(![]() )互为同分异构体
)互为同分异构体
科目:高中化学 来源: 题型:
【题目】下列关于纯净物、混合物、电解质、非电解质的正确组合为( )
纯净物 | 混合物 | 电解质 | 非电解质 | |
A | 盐酸 | 水煤气 | 硫酸 | 干冰 |
B | 蒸馏水 | 蔗糖溶液 | 氧化铝 | 二氧化硫 |
C | 胆矾 | 盐酸 | 铁 | 碳酸钙 |
D | 胆矾 | 水蒸气 | 氯化铜 | 碳酸钠 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卫生部曾发布公告:禁止在面粉生产过程中添加过氧化钙(CaO2)等食品添加剂。下列有关过氧化钙(CaO2)的叙述错误的是
A. CaO2具有氧化性,对面粉可能具有增白作用
B. 过氧化钙固体中阴阳离子个数之比为2:1
C. CaO2和CO2反应时,每产生1molO2转移2mol电子
D. CaO2和水反应的化学方程式为:2CaO2+2H2O═2Ca(OH)2+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列曲线图(纵坐标为沉淀的量,横坐标为加入物质的量)与对应的选项相符合的是( )


A.向1 L浓度均为0.1 mol·L-1的Ba(OH)2、NaAlO2混合溶液中加入0.1 mol·L-1的稀H2SO4
B.向1 L浓度分别为0.1 mol·L-1和0.3 mol·L-1的AlCl3、NH4Cl的混合溶液中加入0.1 mol·L-1的稀NaOH溶液
C.向烧碱溶液中滴加明矾溶液
D.向AlCl3溶液中滴加过量氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)工业上常以氨气为原料制备硝酸,其中有一步非常重要的反应为
4NH3+5O2![]() 4NO+6H2O,该反应的氧化剂为______,还原剂为______。用单线桥法表示该氧化还原反应电子转移的方向和数目____________________________________。
4NO+6H2O,该反应的氧化剂为______,还原剂为______。用单线桥法表示该氧化还原反应电子转移的方向和数目____________________________________。
若有标准状况下VL氨气完全反应,并转移n个电子,则阿伏伽德罗常数(NA)可表示为__________________(写出含n、V的表达式)。
(2)某一反应体系中有反应物和生成物共5种物质:S、 H2S、HNO3、NO、H2O。已知硝酸是一种反应物,该反应中还原产物是________;若反应中转移了0.3mol电子,则氧化产物的质量是_____g。
(3)按要求填空:
①除去碳酸氢钠溶液中的碳酸钠______________________(用离子方程式表示原理);
②除去碳酸钠溶液中的碳酸氢钠,应加试剂为________________;
③用氢氧化钡除去明矾溶液中的硫酸根__________________(用离子方程式表示原理)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用相关原理,回答问题:
Ⅰ.(1)25℃时,水的离子积Kw值为____________。
(2)在T℃的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L,x与y的关系如图所示:

①T℃下,水的离子积为_______________。
②T℃下,0.01 mol/L NaOH溶液中c(H+) 为____________mol/L。
Ⅱ.25℃时,电离平衡常数如下。回答下列问题:
化学式 | CH3COOH | H2S | HClO |
电离平衡常数 | 1.8×10-5 | K1=1.3×10-7 K2=7.1×10-15 | 3.0×10-8 |
(1)物质的量浓度均为0.1mol/L的下列四种物质:
a.Na2S b.NaClO c.CH3COONa d.NaHS
pH由大到小的顺序是____________________(填序号)。
(2)25℃时,0.1 mol/L的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是___________________。
a.c(H+) b.c(H+)/c(CH3COOH) c.c(H+)·c(OH-)
(3)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中 c(CH3COO-)-c(Na+)=______________mol/L(填数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上电解制碱的技术是用离子交换膜法。请回答下列问题:
(1)电解精制食盐水,电解槽中的阳离子交换膜把电解槽隔成了阴极室和阳极室,它只允许阳离子通过,而不允许_____________(填离子符号)和气体通过。
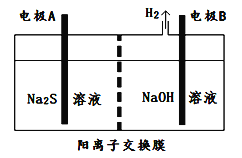
(2)氯碱工业中获得的烧碱可以吸收有毒气体H2S,吸收后的溶液加入到如图所示的电解池的阳极区进行电解以获取单质硫。
①Na2S溶液显碱性的原因(离子方程式):____________________________________________________________。
②电极A应该与直流电源的____________相连。A电极反应为________________________________________________。
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节电、节能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出。
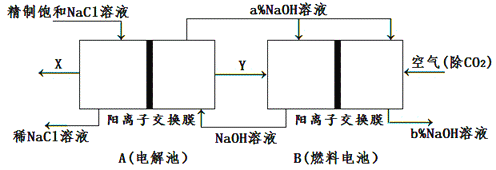
①图示中电极产物X、Y分别是____________、____________(填化学式)。图示中氢氧化钠溶液质量分数大小:a%______b%(填“﹥”“﹤”或“=”)。
②燃料电池B中正极的电极反应:_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质用途的叙述中不正确的是( )
A.钠和钾的合金可用于快中子反应堆作热交换剂
B.FeCl3溶液能与Cu反应,可用于蚀刻印刷电路板
C.明矾溶于水后能产生Al(OH)3胶体,可用作净水剂
D.在医疗上,可用碳酸钠治疗胃酸过多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以反应5H2C2O4+2MnO4-+6H+===10CO2↑+2Mn2++8H2O为例探究“外界条件对化学反应速率的影响”。实验时,分别量取H2C2O4溶液和酸性KMnO4溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。
编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | ||
① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
下列说法不正确的是
A. 实验①、②、③所加的H2C2O4溶液均要过量
B. 实验①测得KMnO4溶液的褪色时间为40 s,则这段时间内平均反应速率υ(KMnO4)=2.5×10-4mol·L-1·s-1
C. 若生成a L CO2(标准状况),该反应转移的电子数为aNA/22.4
D. 实验①和②起初反应均很慢,过了一会儿速率突然增大,可能是生成的Mn2+对反应起催化作用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com