
| A. | 氘(D)的原子核外有2个电子 | |
| B. | 1H与D是同一种原子 | |
| C. | H2O与D2O互称同素异形体 | |
| D. | 1H${\;}_{2}^{18}$O与D${\;}_{2}^{16}$O的相对分子质量相同 |
分析 A.原子的核外电子数等于质子数;
B.核素是指具有一定数目质子和一定数目中子的一种原子;
C.同种元素形成的不同单质互为同素异形体;
D.依据所给原子的质量数分别计算相对分子质量,据此分析.
解答 解:A.氘(D)原子内有1个质子,原子的核外电子数等于质子数,核外有1个电子,故A错误;
B.1H与D是氢元素的2种不同原子,故B错误;
C.H2O与D2O均为水,属于化合物,不互为同素异形体,故C错误;
D.1H218O的相对分子质量为:1×2+18=20,D216O的相对分子质为2×2+16=20,故D正确;
故选D.
点评 本题考查同素异形体及同位素,把握相关的概念及核变化为解答的关键,注重基础知识的考查,题目难度不大.


 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:选择题
| A. | 2 mol•L-1 | B. | 0.2 mol•L-1 | C. | 0.02mol•L-1 | D. | 20 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
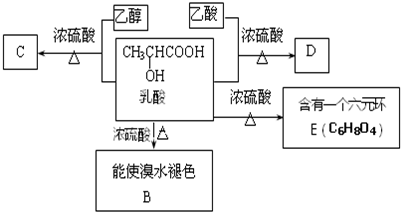
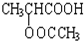 ;
;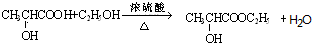 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
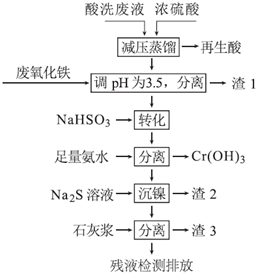
| Fe3+ | Ni2+ | Cr3+ | |
| 开始沉淀 | 1.5 | 6.7 | 4.0 |
| 沉淀完全 | 3.4 | 9.5 | 6.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
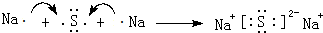
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若3<m<8,则X必定为主族元素 | |
| B. | 若a<b且m=n=4,X、Y不可能形成化合物 | |
| C. | Y的气态氢化物的分子式为H8-nY | |
| D. | 若a=b=3,8>m>n>5,则元素非金属性:X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu→CuCl2 | B. | CuO→Cu2O | C. | Cu(OH)2→CuO | D. | CuO→Cu(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com