
【题目】A、B、C三种金属,A中混有C时A先腐蚀,A与B组成原电池,A为电池正极,则A、B、C三种金属的活动性顺序为
A.A>B>C B.A>C>B C.B>A>C D.B>C>A
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】实验室将化学式为 C8H16O2的酯水解,得到A和B两种物质, A 氧化可转变为 B,符合上述性质的酯的结构种类有( )
A. 1 种 B. 2 种 C. 3 种 D. 4 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在海水的综合利用中,海水提溴工业是一个重要组成部分,其中一种提溴的工艺是在预先浓缩并酸化的海水中,通入足量氯气,然后使生成的溴与吸收剂SO2反应转化为氢溴酸以达到富集溴元素的目的。在有关上述工艺流程的以下化学用语中,错误的是( )
A. 用电子式表示氢溴酸的形成过程为![]()
B. 海水中Br的电子式为:![]()
C. 海水中通入氯气时反应的离子方程式:2Br-+Cl2==Br2+2Cl-
D. Cl-的结构示意图为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修3物质结构与性质] T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表。
元素 | 相关信息 |
T | T元素可形成自然界硬度最大的单质 |
W | W与T同周期,核外有一个未成对电子 |
X | X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/molkJ/mol,I4=11575kJ/mol |
Y | 常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质 |
Z | Z的一种同位素的质量数为63,中子数为34 |
(1)TY2是一种常用的溶剂,是 (填极性分子或非极性分子),分子中存在 个σ 键。W的最简单氢化物容易液化,理由是 。
(2)在25℃、101kpa下,已知13.5g的X固体单质在O2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为 。
(3)基态Y原子中,电子占据的最高能层符号 ,该能层具有的原子轨道数为 、电子数为 。Y、氧、W元素的第一电离能由大到小顺序为 (用元素符号作答)。
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00 g/cm3,则晶胞边长为 ;ZYO4常作电镀液,其中YO42-的空间构型是 ,其中Y原子的杂化轨道类型是 。元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2=ZCl+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是
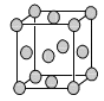
A.O2是 氧化剂
B.HO2 是氧化产物
C. HO2在碱中能稳定存在
D.1 mol Z参加反应有1 mol电子发生转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼是第IIIA族元素,单质硼在加热条件下能与多种非金属反应。某同学欲利用氯气和单质硼反应制备三氯化硼。已知BCl3的沸点为12.5℃,熔点为-107.3℃,遇水剧烈反应。
(1)选用下图所示的装置(可以重复选用)进行实验,装置依次连接的合理顺序为________。

(2)图中g管的作用是______,装置E的作用是_______。
(3)开始实验时,先点燃____(填“A”或“B”)处的酒精灯。
(4)请写出BCl3遇水变质的化学方程式___________。
(5)硼酸是一元弱酸,其钠盐化学式为Na[B(OH)4],则硼酸在水中电离方程式是______。
(6)实验完成后,某同学向F (溶液中含有0.05 mol/LNaC10、0.05 mol/LNaCl、0.1 mol/L NaOH)中滴加品红溶液,发现溶液褪色。现设计实验探究溶液褪色的原因,请将表中数据补充完整,完成实验方案。
实验序号 | 0.1mol/LNaClO溶液/mL | 0.1mol/LNaCl溶液/mL | 0.2mol/LNaOH溶液/mL | H2O /mL | 品红溶液 | 现象 |
① | 4.0 | 0 | 0 | x | 3滴 | 较快褪色 |
② | 0 | 4.0 | 4.0 | 0 | 3滴 | 不褪色 |
③ | 4.0 | 0 | 4.0 | 0 | 3滴 | 缓慢褪色 |
x=_______,结论:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】端炔烃在催化剂存在下可发生偶联反应,成为Glaser反应。
2R—C≡C—H![]() R—C≡C—C≡C—R+H2
R—C≡C—C≡C—R+H2
该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应制备化合物E的一种合成路线:

回答下列问题:
(1)A的分子式为C6H6,则A和B的关系互为_____________________。
(2)B的化学名称为_________,D 中官能团的电子式的为____________________________。
(3)②和③的反应类型分别为___________________________、___________________________________________。
(4)E的结构简式为______________________________。
(5)反应①的化学方程式为________________________________________________________________________。
(6)化合物(![]() )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为________________________________________________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为________________________________________________________________________。
(7)写出用2苯基乙醇为原料(其他无机试剂任选)制备化合物D的流程图__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是乙酸乙酯的合成路线图,已知B的水溶液可以溶解CaCO3,E可作果实催熟剂。
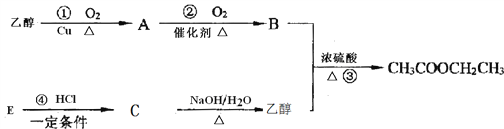
请完成下列问题:
(1)A的名称是_______;B中所含的官能团是__________;E的结构简式为___________________ 。
(2)反应③的反应类型是________;反应④的反应类型是_________________。
(3)写出CH3COOCH2CH3的同分异构体(含有酯基)______________________。
(4)请写出以下反应化学方程式:
A、合成路线①的方程式为____________________;
B、成路线④的方程式为_____________________;
C、物质E在一定条件下发生加聚反应的化学反应方程为___________________________;
D、写出乙酸乙酯在NaOH溶液中的水解反应方程式______________________;
E、写出B的水溶液溶解CaCO3的方程式________________________。
(5)如果用4.6 g的乙醇和9.0 g的B反应制得乙酸乙酯5.28 g。则本实验的产率是:__________(产率指的是某种生成物的实际产量与理论产量的比值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2 L的密闭容器中,X、Y、Z三种气体随时间变化的曲线如图所示。
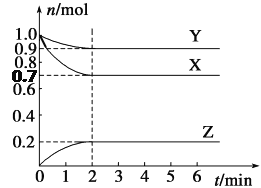
请回答下列问题:
(1)由图中数据分析:该反应的化学方程式为__________________________。
(2)反应开始至2 min,Z的平均反应速率为________。
(3)5 min时Z的生成速率与6 min时Z的生成速率相比较,前者________后者(填“大于”、“小于”或“等于”)。
(4)上述反应过程中,如果降低温度,则其反应速率________(填“增大”、“减小”或“不变)。如果使用合适的催化剂,则其反应速率________ (填“增大”、“减小”或“不变)。
(5)下列各项中不可以说明上述反应达到平衡的是________(填字母)。
a.混合气体的密度不变
b.混合气体的压强不变
c.同一物质的正反应速率等于逆反应速率
d.X的浓度保持不变
e.生成1 mol Z和同时生成1.5 mol X
f.X、Y、Z的反应速率之比为3∶1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列填空。
(1)下列几组物质中,互为同分异构体的是________;互为同系物的是________。
A.CH2=CH-COOH和油酸(C17H33COOH)
B.12C60和石墨
C.乙醇和乙二醇
D.35Cl和37Cl
E.![]() 和
和![]()
(2)下图是某有机物的球棍模型,该有机物的分子式为_________;名称为________。

(3)在有机化学分析中,根据反应的性质和反应产物,即可确定烯烃的组成和结构(双键及支链的位置),例如:

据以上线索和下列反应事实,确定C7H14的结构和名称:

该烃的结构筒式为_____________,名称是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com