


科目:高中化学 来源: 题型:
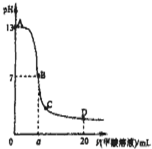 向15mL 0.1mol?L-1KOH溶液中逐滴加入0.2mol?L-1甲酸(HCOOH,一元弱酸)溶液,溶液pH和加入的甲酸的体积关系曲线如右图所示,有关粒子浓度大小关系正确的是( )
向15mL 0.1mol?L-1KOH溶液中逐滴加入0.2mol?L-1甲酸(HCOOH,一元弱酸)溶液,溶液pH和加入的甲酸的体积关系曲线如右图所示,有关粒子浓度大小关系正确的是( )| A、在A、B间任意一点c(K+)>c(HCOO-)>c(OH-)>c(H+) |
| B、在B点:c(K+)=c(HCOO-)>c(OH-)=c(H+),且a=7.5 |
| C、在C点:c(HCOO-)>c(K+)>c(OH-)>c(H+) |
| D、在D点:c(HCOO-)+c(HCOOH)>2c(K+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4和C2H4 |
| B、C2H2和C2H4 |
| C、C2H4和C2H6 |
| D、C3H4和C3H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾溶液可以对自来水进行净水 |
| B、电解法精炼粗铜,纯铜做阴极 |
| C、铅蓄电池的负极是Pb |
| D、增大压强平衡一定发生移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
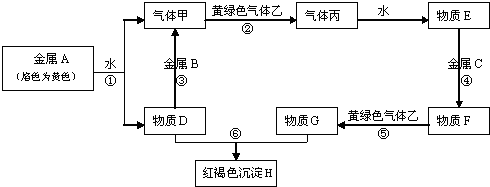
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3溶液中加入过量氨水 |
| B、Al2(SO4)3溶液中加入过量KOH溶液 |
| C、MgCl2溶液中加入过量氢氧化钠 |
| D、澄清石灰水中通入过量CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
查看答案和解析>>
科目:高中化学 来源: 题型:
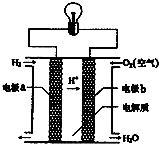
| A、a极是正极,b极是负极 |
| B、该装置能将化学能转化为电能 |
| C、电子由a极通过导线流向b极 |
| D、供电时总反应为2H2+O2=2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、MgO+2H+=Mg2++H2O |
| B、CO32-+2H+=CO2↑+H2O |
| C、OH-+H+=H2O |
| D、CaCO3+H+=Ca2++CO2↑+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com