
| A. | ①②③ | B. | ①③⑤ | C. | ②③⑤ | D. | ②④⑤ |
分析 既能与氢氧化钠溶液反应又能与盐酸反应,且在生成物中都有盐和水,常见物质有:两性氧化物、两性氢氧化物、弱酸酸式盐、弱酸的铵盐等,据此进行解答.
解答 解:①Al与氢氧化钠溶液反应生成偏铝酸钠与氢气,与盐酸反应生成氯化铝与氢气,没有水生成,故①错误;
②Al(OH)3与氢氧化钠反应生成偏铝酸钠与水,与盐酸反应生成氯化铝与水,故②正确;
③Al2O3与氢氧化钠反应生成偏铝酸钠与水,与盐酸反应生成氯化铝与水,故③正确;
④MgCO3与氢氧化钠反应生成氢氧化镁和碳酸钠,没有水生成,故④错误;
⑤NaHCO3与氢氧化钠反应生成碳酸钠与水,与盐酸反应生成氯化钠、水与二氧化碳,故⑤正确;
故选C.
点评 本题考查元素化合物性质,难度不大,侧重对基础知识的巩固,注意归纳总结中学常见的既能与酸反应又能与碱反应的物质.


科目:高中化学 来源: 题型:选择题
| A. | K2SO4溶液 | B. | KNO3溶液 | C. | Na2SO4(s) | D. | Na2CO3(s) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 弱酸酸式盐 NaHB 在水溶液中水解:HB-+H2O?H3O++B2- | |
| B. | 工业上电解饱和食盐水:C1-+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+OH- | |
| C. | AlCl3溶液与小苏打溶液混合:Al3++3HCO3-═Al(OH)3↓+3CO2↑ | |
| D. | FeBr2溶液中通入过量 Cl2:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③>④>②>① | B. | ④>③>②>① | C. | ①>④=③>② | D. | ③=④>①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
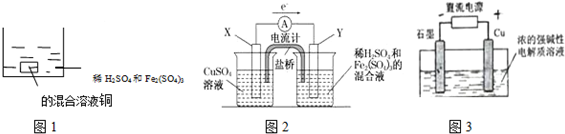
| A. | 如图1 所示将一定量的铜片加入到100 mL 稀硫酸和硫酸铁的混合溶液中,若铜片完全溶解时(不考虑盐的水解及溶液体积的变化),溶液中的Fe3+、Cu2+、H+三种离子的物质的量浓度相等,且测得溶液的pH=1,则溶液中c(SO42-)为0.5mol/L | |
| B. | 如图2 所示的装置中发生Cu+2Fe3+═Cu2++2Fe2+的反应,X 极是负极,Y 极的材料名称可以是铜 | |
| C. | Cu2O 是一种半导体材料,基于绿色化学理念设计的制取.Cu2O 的电解池示意图如图3所示,石墨电极上产生氢气,铜电极发生还原反应 | |
| D. | 如图3 所示当有0.1mol 电子转移时,有0.1molCu2O 生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com