
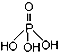
 ),次磷酸钠(NaH2PO2)可用于化学镀镍等等.完成下列填空:
),次磷酸钠(NaH2PO2)可用于化学镀镍等等.完成下列填空:分析 (1)NaH2PO2中涉及到四种元素为Na、H、P和O,原子的电子层数越多,原子半径越大,若电子层相同,核电荷数越大,原子半径越小;
(2)根据磷元素所在的周期及离子电子层越少、核电荷数越大离子半径越小判断满足条件的元素名称,写出其最高价氧化物对应的水化物的电离方程式;
(3)磷酸二氢钠在溶液中存在水解和电离两个过程,溶液显示酸性,说明磷酸二氢根离子电离程度大于其水解程度;
(4)根据氧化还原反应中化合价变化及质量守恒定律判断反应物和生成物,并配平反应方程式、判断还原产物,依据化学反应方程式计算转移电子数.
解答 解:(1)NaH2PO2中含有的元素中,H原子电子层最少,原子半径最小,其次是氧原子的原子半径,钠原子和磷原子都含有三个电子层,磷原子的核电荷数大于钠原子,所以磷原子的原子半径小于钠原子,所以它们的原子半径关系为H<O<P<Na,
故答案为:H<O<P<Na;
(2)磷位于第三周期,第三周期中阳离子失去电子,电子层减少一层,离子半径最小,离子的核电荷数越大,离子半径越小,所以铝离子的半径最小;铝元素最高价氧化物对应的水化物为氢氧化铝,其电离方程式为:H++AlO2-+H2O?Al(OH)3?Al3++3OH-,
故答案为:H++AlO2-+H2O?Al(OH)3?Al3++3OH-;
(3)磷酸二氢钠的溶液中,磷酸二氢根离子电离程度大于水解程度,所以其水溶液显示酸性,
故答案为:磷酸二氢根离子电离程度大于水解程度;
(4)由氧化还原反应中化合价升降相等进行配平:镍元素的化合价降低了2价,磷元素的化合价升高的2价,根据原子守恒结合电荷守恒可得配平的方程式为:H2O+Ni2++H2PO2-═Ni+H2PO3-+2H+,镍离子被还原成金属Ni,还原产物为Ni,此过程转移2mol电子,故反应中转移1摩尔电子时,理论上产生金属镍59×$\frac{1}{2}$=29.5克,
故答案为:1;1;H2O;1;1;2H+;Ni;29.5.
点评 本题考查了原子结构与元素性质的关系、氧化还原反应的配平、粒子半径大小比较等知识,题目难度中等,试题涉及的内容较多,题量较大,充分考查了学生的分析能力及灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 反应①、②、③都是氧化还原反应 | |
| B. | 反应①中H2O2被还原 | |
| C. | 氧化性:KMnO4>O2 | |
| D. | 每生成1mol F2,上述反应共转移2mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 2min | 4min | 6min | 8min | … | |
| CO | 0.07 | 0.06 | 0.06 | 0.05 | … |
| H2 | x | 0.12 | 0.12 | 0.2 | … |
| CH3OH | 0.03 | 0.04 | 0.04 | 0.05 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤⑥ | B. | ④⑥⑦ | C. | ③④⑦ | D. | 以上都不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 35.5:108 | B. | 16:137 | C. | 8:1 | D. | 108:35.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 的合成路线如图(部分反应条件省略)
的合成路线如图(部分反应条件省略)
 (注明反应的条件).
(注明反应的条件). .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | C-O | C$\stackrel{←}{=}$O | H-O | C-H |
| E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com