
【题目】0.05 mol某金属单质与足量的盐酸反应,放出1.68LH2(标准状况),并转变为具有Ne原子的电子层结构的离子,该金属元素在元素周期表中的位置是( )
A. 第三周期第IA族B. 第三周期第ⅢA族
C. 第三周期第ⅡA族D. 第四周期第IA族
科目:高中化学 来源: 题型:
【题目】关于过氧化物的叙述正确的是(NA表示阿伏伽德罗常数)( )
A. 7.8g过氧化钠含有的共用电子对数为0.2NA
B. 2H2O2(l)=2H2O(l)+O2(g)ΔH=98.2 kJ/mol,ΔS=70.5 J/mol·K,该反应低温能自发进行
C. 过氧化氢使高锰酸钾溶液褪色,1mol过氧化氢得到2NA电子
D. 在含有NH4+、Ba2+、Cl—、NO3—离子的溶液 加入少量过氧化钠以上各离子量几乎不减少
【答案】B
【解析】
A.过氧化钠的电子式为![]() ,则7.8g过氧化钠含有的共用电子对为
,则7.8g过氧化钠含有的共用电子对为![]() ×1=0.1mol,故A错误;B.2H2O2(l)=2H2O(l)+O2(g)△H=-98.2kJmol-1,△S=70.5Jmol-1K-1,则△G=△H-T△S<0在任何温度下都小于0,故B正确;C.过氧化氢遇强氧化剂酸性高锰酸钾溶液时,过氧化氢中的氧元素的化合价是-1价可升高为0价,发生还原反应,所以1mol过氧化氢失去2NA电子,故C错误;D.过氧化钠与水反应生成氢氧化钠和氧气,氢氧根与NH4+反应生成氨水,所以NH4+会减小,故D错误;故选B。
×1=0.1mol,故A错误;B.2H2O2(l)=2H2O(l)+O2(g)△H=-98.2kJmol-1,△S=70.5Jmol-1K-1,则△G=△H-T△S<0在任何温度下都小于0,故B正确;C.过氧化氢遇强氧化剂酸性高锰酸钾溶液时,过氧化氢中的氧元素的化合价是-1价可升高为0价,发生还原反应,所以1mol过氧化氢失去2NA电子,故C错误;D.过氧化钠与水反应生成氢氧化钠和氧气,氢氧根与NH4+反应生成氨水,所以NH4+会减小,故D错误;故选B。
【题型】单选题
【结束】
19
【题目】常温下,现向50 mL 0.1 mol·L-1 NH4HSO4溶液中滴加0.05 mol·L-1 NaOH溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生)。下列说法正确的是

A. b点溶液中离子浓度由大到小的顺序为: c(Na+)>c(SO42—)>c(NH4+)>c(H+)>c(OH-)
B. 图中b、c、d 三点溶液中水的电离程度最大的是c点
C. b点后滴加NaOH溶液过程中,NH3·H2O的电离程度逐渐减小
D. pH=7时,溶液中c(H+)+c(Na+)+c(NH4+)=c(SO42—)+c(OH-)
【答案】C
【解析】
试题A.b点表示NH4HSO4溶液与NaOH溶液恰好反应生成硫酸钠、硫酸铵,溶液显酸性,离子浓度由大到小的顺序为:c(Na+)=c(SO![]() )>c(NH
)>c(NH![]() )>c(H+)>c(OH-),故A错误;B.图中b点硫酸铵水解,促进水的电离、c点显中性,生成了部分NH3·H2O,抑制了水的电离、d点氢氧化钠过量,抑制水的电离,三点溶液中水的电离程度最大的是a点,故B错误;C.b点后滴加NaOH溶液过程中,NH3·H2O的浓度逐渐增大,电离程度逐渐减小,故C正确;D.pH=7时,溶液中存在电荷守恒c(H+)+c(Na+)+c(NH
)>c(H+)>c(OH-),故A错误;B.图中b点硫酸铵水解,促进水的电离、c点显中性,生成了部分NH3·H2O,抑制了水的电离、d点氢氧化钠过量,抑制水的电离,三点溶液中水的电离程度最大的是a点,故B错误;C.b点后滴加NaOH溶液过程中,NH3·H2O的浓度逐渐增大,电离程度逐渐减小,故C正确;D.pH=7时,溶液中存在电荷守恒c(H+)+c(Na+)+c(NH![]() )=2c(SO
)=2c(SO![]() )+c(OH-),故D错误;故选C。
)+c(OH-),故D错误;故选C。
考点:考查了弱电解质的电离平衡、离子浓度的大小比较的相关知识。
【题型】单选题
【结束】
20
【题目】下列有关电解质溶液的说法正确的是
A.Na2SO3溶液加水稀释后,pH和KW均减小
B.0.1molL﹣1Na2CO3溶液中:c(OH﹣)=c(H+)+c(HCO3﹣)+2c(H2CO3)
C.浓度分别为0.2molL﹣1和0.1molL﹣1的CH3COOH溶液中,c(H+)之比等于2:1
D.室温下,PH=12的氨水与PH=2的H2SO4溶液等体积混合后,溶液呈酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积固定的2L密闭容器中,一定条件下发生如下反应:X(g)+2Y(g)nZ(g),反应过程中各物质的量与时间的关系如图所示.完成下列填空:
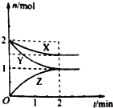
(1)n=______;
(2)Y的平衡浓度为_______;
(3)反应开始至平衡,X 的反应速率v(X)=______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下图所示装置制备干燥纯净的氯气,并进行氯气的性质实验,请回答下列问题:
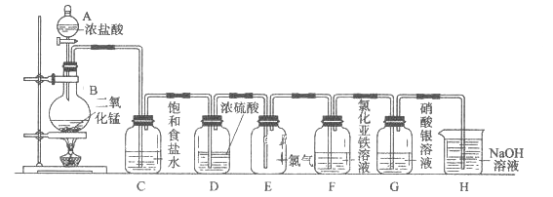
(1)A中盛有浓盐酸,B中盛有MnO![]() ,则烧瓶中发生反应的化学方程式为:______。
,则烧瓶中发生反应的化学方程式为:______。
(2)C中盛有饱和食盐水,其作用是_________,装置D的作用_________。
(3)装置E中气体的颜色为_______,E中Cl![]() 能使湿润的红色布条褪色的原因是________。
能使湿润的红色布条褪色的原因是________。
(4)F中是FeCl![]() 溶液,现象是________,发生反应的离子方程式为__________。
溶液,现象是________,发生反应的离子方程式为__________。
(5)G中是AgNO![]() 溶液,现象是___________,有关化学反应的离子方程式为_________。
溶液,现象是___________,有关化学反应的离子方程式为_________。
(6)H中盛有NaOH溶液,其作用是_______,发生反应的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)从樟科植物枝叶提取的精油中含有下列甲、乙、丙三种成分:

丙
分子式 | C16H14O2 |
部分性质 | 能使Br2/CCl4褪色 |
能在稀H2SO4中水解 |
(1)甲中含氧官能团的名称为________。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):

其中反应Ⅰ的反应类型为________,反应Ⅱ的化学方程式为_______________(注明反应条件)。
(3)已知:RCH===CHR′![]() RCHO+R′CHO;2HCHO
RCHO+R′CHO;2HCHO![]() HCOOH+CH3OH
HCOOH+CH3OH
由乙制丙的一种合成路线图如下(A~F均为有机物,图中Mr表示相对分子质量):

①下列物质不能与C反应的是________(选填序号)。
a.金属钠 b.HBr c.Na2CO3溶液 d.乙酸
②写出F的结构简式__________________________________。
③丙有多种同分异构体,写出能同时满足下列条件的同分异构体________。
a.苯环上连接三种不同官能团
b.能发生银镜反应
c.能与Br2/CCl4发生加成反应
d.遇FeCl3溶液显示特征颜色
④综上分析,丙的结构简式为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(ClNO)参与大气平流层和对流层的化学,气相的ClNO光解和水解都可产生Cl自由基。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及的化
学反应、对应的反应热和平衡常数如表:
化学反应 | 反应热 | 平衡常数 |
①2NO2(g)+NaC1(s) | △H1 | K1 |
②2NO(g)+C12(g) | △H2 | K2 |
③4NO2(g)+2NaC1(s) | △H3 | K3 |
则K1,K2,K3之间的关系为K2=______________,△H3=_____________
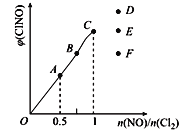
(2)已知2NO(g)+Cl2(g)![]() 2ClNO(g),一定条件下在恒温恒容的密闭容器中按一定比例,充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(C12)的变化图象如图,则A、B、C三状态中,NO的转化率最大的是___点,当n(NO)/n(C12)=1.5时,达到平衡状态ClNO的体积分数可能是D、E、F三点中的_____点。
2ClNO(g),一定条件下在恒温恒容的密闭容器中按一定比例,充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(C12)的变化图象如图,则A、B、C三状态中,NO的转化率最大的是___点,当n(NO)/n(C12)=1.5时,达到平衡状态ClNO的体积分数可能是D、E、F三点中的_____点。
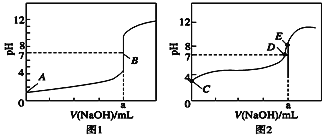
(3)常温下,用0.100 0 mol·L-1 NaOH溶液分别滴定20.00 mL 0.100 0 mol·L-1 HBr溶液和20.00 mL0.100 0 mol·L-1 CH3COOH溶液,得到2条滴定曲线,如图所示:
①根据图1和图2判断,滴定HBr溶液的曲线是______________(填“图1”或“图2”);
②a=______ mL; ③c(Na+)=c(CH3COO-)的点是______点;
④E点对应溶液中离子浓度由大到小的顺序为_______________。
(4) 氨气燃料电池,一极通入氨气,另一极通入空气,电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,它在熔融状态下能传导O2-。写出负极的电极反应式_____________。
(5) 已知:CdCO3、NiCO3溶度积分别为6.0×10-12、1.0×10-7。p(CO32-)=-lg c(CO32-) 。在含Cd2+、Ni2+浓度均为0.01 mol/L的废水中滴加稀碳酸钠溶液。为了分离这两种阳离子,需要控制p(CO32-)范围为_____________(忽略溶液体积的变化)
A.4≤p(CO32-)≤6
B.5<p(CO32-)≤ 7-lg6
C.7-lg6<p(CO32-)≤ 8
D.7<p(CO32-)≤8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关氧化还原反应的理解正确的是( )
A. 在一定条件下,氯酸钾与碘发生反应KClO3+I2=2KIO3+Cl2 由此判断氧化性 I2>Cl2
B. 已知反应:2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O其中1mol氧化剂在反应中得到的电子为12 mol
C. (NH4)2SO4在高温下分解生成 SO2、H2O、N2和 NH3。则该反应的氧化产物:还原产物=1:3
D. 在反应2CuFeS2 + O2 = Cu2S + 2FeS + SO2中,若有1molO2参加反应,则反应中有4mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
选项 | 被提纯物质 | 杂质 | 除杂试剂或方法 |
A | FeCl3溶液 | FeCl2 | 通入适量Cl2 |
B | Cl2 | H2O (蒸气) | 通入浓硫酸中 |
C | 铜粉 | 铁粉 | 加入过量盐酸并过滤 |
D | CO2 | HCl | 通入饱和的碳酸钠溶液中 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,二氯化二硫(S2Cl2)为橙黄色液体,遇水易水解,工业上用于橡胶的硫化。某学习小组用氯气和硫单质合成S2Cl2的实验装置如图所示.下列说法正确的是
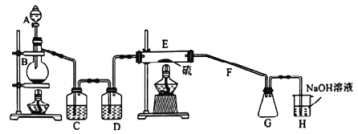
A. 实验时需先点燃E处的酒精灯
B. C、D中所盛试剂为饱和氯化钠溶液、浓硫酸
C. 二氯化二硫(S2Cl2)水解反应产物为:S、H2S、HCl
D. G中可收集到纯净的产品
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com