
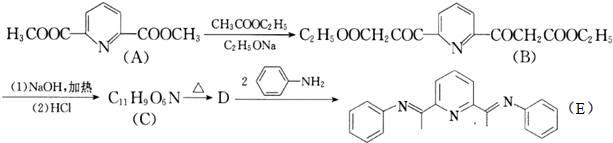
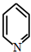
 )且环上只有2个取代基;
)且环上只有2个取代基;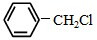 和
和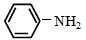 为原料合成西佛碱N-苯基苯甲亚胺(
为原料合成西佛碱N-苯基苯甲亚胺(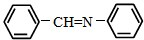 ),请你拟出合成路线:
),请你拟出合成路线: ,比较C的分子式和D的结构,结合C是B水解再酸化得到的,可以确定C为
,比较C的分子式和D的结构,结合C是B水解再酸化得到的,可以确定C为 ,据此答题.
,据此答题. ,比较C的分子式和D的结构,结合C是B水解再酸化得到的,可以确定C为
,比较C的分子式和D的结构,结合C是B水解再酸化得到的,可以确定C为 ,
, )且环上只有2个取代基;
)且环上只有2个取代基; ,
, ;
; ,
, ;
;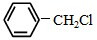 和
和 为原料合成西佛碱N-苯基苯甲亚胺(
为原料合成西佛碱N-苯基苯甲亚胺(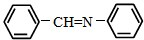 ),应先将
),应先将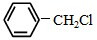 碱性水解,氯原子换成羟基,再氧化成醛基,利用题中D→E的信息,与苯胺反应得产物,合成路线为
碱性水解,氯原子换成羟基,再氧化成醛基,利用题中D→E的信息,与苯胺反应得产物,合成路线为 ,
, .
.


科目:高中化学 来源: 题型:
| 滴定次数 | 待测液体积(mL) | 标准酸液的体积 | |
| 滴定前刻度(mL) | 滴定后刻度(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某学生欲用已知物质的量浓度为0.1000mol/L的NaOH溶液来测定未知物质的量浓度的盐酸,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度为0.1000mol/L的NaOH溶液来测定未知物质的量浓度的盐酸,选择酚酞作指示剂.请填写下列空白:| 实验 编号 | NaOH溶液的 浓度/mol?L-1 | 滴定完成时,溶液滴入的体积/mL aOH | 待测盐的体积/mL酸 |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 定”).
定”).查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 -OH和
-OH和 CH2OHE.NH2CH2COOH与NH2CH(CH3)COOHF.CH3CHO与CH2=CHCHO.
CH2OHE.NH2CH2COOH与NH2CH(CH3)COOHF.CH3CHO与CH2=CHCHO.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com