
科目:高中化学 来源:2015-2016学年甘肃省高二上期末化学试卷(解析版) 题型:选择题
室温下向10mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
A.溶液中所有粒子的浓度都减少
B.溶液中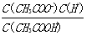 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10mL pH=11的NaOH溶液,混合液pH=7
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二下期末化学试卷(解析版) 题型:填空题
科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图如图1可简单表示如下,其中配位键和氢键均采用虚线表示。
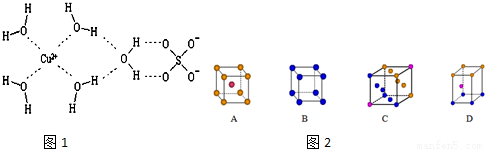
(1)金属铜采用下列______________堆积方式。
(2)Cu2+还能与NH3、Cl-等形成配位数为4的配合物。
①[Cu(NH3)4]2+中存在的化学键类型有______________(填序号)。
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
②元素金(Au)处于周期表中的第六周期,与Cu同族,一种铜合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为______________;
(3)在硫酸铜溶液中逐滴滴加氨水至过量,先出现蓝色沉淀,最后溶解形成深蓝色溶液.写出此蓝色沉淀溶解的离子方程式:______________;
(4)向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成血红色.该反应在有的教材中用方程式FeCl3+3KSCN═Fe(SCN)3+3KCl表示.经研究表明,Fe(SCN)3是配合物,Fe3+与SCN-不仅能以1:3的个数比配合,还可以其他个数比配合.请按要求填空:
①Fe3+与SCN-反应时,Fe3+提供______________,SCN-提供______________,二者通过配位键结合.
②所得Fe3+与SCN-的配合物中,主要是Fe3+与SCN-以个数比1:1配合所得离子显血红色.含该离子的配合物的化学式是______________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二下期末化学试卷(解析版) 题型:选择题
下列说法不正确的是( )
A.晶体在受热熔化过程中一定存在化学键的断裂
B.晶体的自范性是指在适宜条件下晶体能够自发地呈现规则的多面体外形
C.区分晶体和非晶体最科学的方法是对固体进行X-射线衍射实验
D.晶体的各向异性取决于微观粒子的排列具有特定的方向性
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二下期末化学试卷(解析版) 题型:选择题
以下各分子中,所有原子都满足最外层8电子稳定结构的是( )
A.NO2 B.BF3 C.PCl3 D.H3O+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二下期末化学试卷(解析版) 题型:选择题
瑞典皇家科学院2001年10月10日宣布,2001年诺贝尔化学奖授予在“手性碳原子的催化氢化、氧化反应”研究领域作出贡献的美、日三位科学家.下列分子中不含有“手性碳原子”的是( )
A.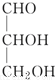
B.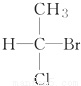
C.CH3CH2OH
D.
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一下期末化学试卷(解析版) 题型:选择题
利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示.下列说法不正确的是( )
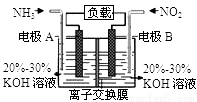
A.电流从右侧电极经过负载后流向左侧电极
B.为使电池持续放电,离子交换膜需选用阴离子交换膜
C.电极A极反应式为:2NH3-6e-=N2+6H+
D.当有4.48L NO2(标准状况) 被处理时,转移电子为0.8mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一下期末化学试卷(解析版) 题型:选择题
下列操作或装置能达到实验目的是( )
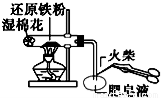
A. 检验铁粉与水蒸气反应产生的氢气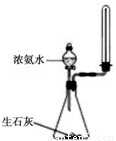
B. 快速制备和收集一定量的氨气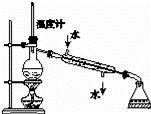
C. 分离互溶但沸点相差较大的液体混合物
D. 除去甲烷中少量的乙烯得纯净甲烷
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省汕头市高一下期末化学试卷(解析版) 题型:填空题
某同学学习了化学反应速率后,联想到曾用H2O2制备氧气,于是设计了下面的实验方案并进行实验探究。
实验编号 | 反 应 物 | 催 化 剂 |
甲 | 试管中加入3 mL 2﹪ H2O2溶液和3滴蒸馏水 | 无 |
乙 | 试管中加入3 mL 5﹪ H2O2溶液和3滴蒸馏水 | 无 |
丙 | 试管中加入3 mL 5﹪ H2O2溶液和3滴蒸馏水 | 1 mL 0.1 mol/L FeCl3溶液 |
丁 | 试管中加入3 mL 5﹪ H2O2溶液和3滴稀盐酸溶液 | 1 mL 0.1 mol/L FeCl3溶液 |
戊 | 试管中加入3 mL 5﹪ H2O2溶液和3滴NaOH溶液 | 1 mL 0.1 mol/L FeCl3溶液 |
【查阅资料】过氧化氢(H2O2),其水溶液俗称双氧水,常温下是一种无色液体,性质比较稳定。在加热的条件下,它能分解生成氧气。研究表明,将新制的5﹪的H2O2溶液加热到65℃时就有氧气放出,加热到80℃时就有较多氧气产生。
(1)上述实验发生反应的化学方程式为 。
(2)实验甲和实验乙的实验目的是 ;
实验丙、实验丁和实验戊的实验目的是 。
(3)请根据该同学查阅的资料分析H2O2的性质,解释实验甲和实验乙能否达到实验目的? 。
(4)实验过程中该同学对实验丙、丁、戊中产生的气体进行收集,并在2分钟内6个时间点对注射器内气体进行读数,记录数据如下表。
时间/s | 20 | 40 | 60 | 80 | 100 | 120 | |
气体体积/mL | 实验丙 | 9.5 | 19.5 | 29.0 | 36.5 | 46.0 | 54.5 |
实验丁 | 8.0 | 16.0 | 23.5 | 31.5 | 39.0 | 46.5 | |
实验戊 | 15.5 | 30.0 | 44.5 | 58.5 | 71.5 | 83.0 | |
①对实验戊,0~20 s的反应速率v1= mL/s,100~120 s的反应速率v2= mL/s。
不考虑实验测量误差,二者速率存在差异的主要原因是 。
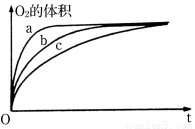
②如右图是根据实验收集到最大体积的气体时所用时间绘制的图像。曲线c表示的是实验 (填“丙”、“丁”或“戊”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com