
【题目】X、Y、Z、W为原子序数递增的短周期主族元素,Y的简单气态氢化物水溶液呈弱碱性, Z元素无正价,且基态原子有2个未成对电子,基态W原子价层电子排布式为nsn-1npn-1 ,X与W为同主族元素。基态R原子M能层全充满且核外有且仅有1个未成对电子。请回答下列问题:
(1)基态R原子的核外电子排布式为____________________。R单质晶体晶胞的堆积方式_______________,晶胞的空间利用率为___________________。
(2) X、Y、Z三种元素的第一电离能由小到大的顺序为__________ (填“元素符号”,下同)
(3)YF3分子中Y的杂化类型为______________。该分子的空间构型为_________________。
(4)Y的气态氢化物在水中可形成氢键,其氢键最可能的形式为___________________。
(5)X的某气态氧化物的相对分子质量为44,分子中的大π键可用符号Π![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则其气态氧化物中的大π键应表示为_______________,其中σ键与π数目之比为______________。
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则其气态氧化物中的大π键应表示为_______________,其中σ键与π数目之比为______________。
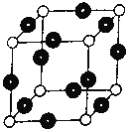
(6)R元素与Y元素形成某种化合物的晶胞结构如图所示(黑球代表R原子),若该晶体的密度为ρg·cm-3,则该晶胞的边长是_________cm (NA表示阿伏伽德罗常数的值)。
【答案】 ls22s22p63s23p63d104sl 面心立方最密堆积 74% C<O<N sp3 三角锥形 B Π![]() 1∶1
1∶1 
【解析】X、Y、Z、W为原子序数递增的短周期主族元素,Y的简单气态氢化物水溶液呈弱碱性,Y为N元素;Z元素无正价,且基态原子有2个未成对电子,Z为O元素;基态W原子价层电子排布式为nsn-1npn-1,则n=3,W为Si元素,X与W为同主族元素,则X为C元素;基态R原子M能层全充满且核外有且仅有1个未成对电子,价层电子排布为3d104s1,R为Cu元素。
(1)基态Cu原子的核外电子排布式为ls22s22p63s23p63d104sl。铜晶体晶胞的堆积方式为面心立方最密堆积,晶胞的空间利用率为74%,故答案为:ls22s22p63s23p63d104sl;面心立方最密堆积;74%;
(2)同一周期,从左到右,元素的第一电离能逐渐增大,但N原子的2p为半充满,均为稳定,第一电离能大于O,C、N、O三种元素的第一电离能由小到大的顺序为C<O<N,故答案为:C<O<N;
(3)NF3分子中N原子上有1个孤对电子,价层电子对数为4,采用sp3杂化,分子的空间构型为三角锥形,故答案为:sp3;三角锥形;
(4)氨气溶于水生成NH3·H2O,能够电离生成铵根离子和氢氧根离子,因此氨气在水中可形成氢键,其氢键最可能的形式为是氨气分子中N原子上的孤对电子与水分子中的H原子共用,形成氢键,故选B;
(5)C的某气态氧化物的相对分子质量为44,该氧化物为二氧化碳,分子中的大π键可用符号Π![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则其气态氧化物中的大π键应表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则其气态氧化物中的大π键应表示为Π![]() ,二氧化碳分子中含有2个C=O,其中σ键与π数目之比为1:1,故答案为:Π
,二氧化碳分子中含有2个C=O,其中σ键与π数目之比为1:1,故答案为:Π![]() ;1∶1;
;1∶1;
(6)根据晶胞中微粒个数的分配方法计算,晶胞中含有N原子的数目为8×![]() =1,Cu原子的数目为:12×
=1,Cu原子的数目为:12×![]() =3,故化学式为Cu3N,1mol晶胞的质量为206g,所以该晶胞的边长=
=3,故化学式为Cu3N,1mol晶胞的质量为206g,所以该晶胞的边长= =
=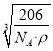 cm,故答案为:
cm,故答案为: 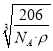 。
。


科目:高中化学 来源: 题型:
【题目】下列说法中错误的是( )
A.从1 L 1 mol/L的NaCl溶液中取出10 mL,其浓度仍是1 mol/L
B.制成0.5 L 10 mol/L的盐酸,需要氯化氢气体112 L(标准状况)
C.0.5 L 2 mol/L BaCl2溶液中,Ba2+和Cl﹣总数为3×6.02×1023
D.10 g 98%的硫酸(密度为1.84 g/cm3)与10 mL 18.4 mol/L硫酸的浓度是不同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氟的卤素互化物通常作氟化剂,使金属氧化物转化为氟化物,如2Co3O4+6C1F3= 6CoF3+3C12+4X。下列有关该反应的说法,正确的是
A. X与O3互为同位素 B. ClF3中氯元素为-3价
C. Co3O4在反应中作氧化剂 D. lmol Co3O4参加反应转移9 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式书写正确的是( )
A.CO2+H2O+CaCl2═2HCl+CaCO3↓
B.2NaCl+MgSO4═Na2SO4+MgCl2
C.2HgO═2Hg+O2
D.2KOH+CO2═K2CO3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸和氢氧化钠是工业上重要的化工原料,也是实验室里常见的试剂.
Ⅰ.测定中和热.
(1)写出稀盐酸和稀氢氧化钠溶液反应表示中和热的热化学方程式 (中和热数值为57.3kJ/mol):
(2)取50mL 0.5mol/L HCl溶液与50mL0.55mol/L NaOH溶液进行测定,但实验数值小于57.3kJ/mol,原因可能是 _(填序号).
A.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度
B.量取盐酸的体积时仰视读数
C.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
D.实验装置保温、隔热效果差
Ⅱ.酸碱中和滴定.
(1)某学生用已知物质的量浓度的盐酸测定未知物质的量浓度的氢氧化钠溶液,选择酚酞作指示剂.实验中不必用到的是
A.酸式滴定管 B.容量瓶 C.锥形瓶 D.铁架台
(2)用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_____________.当________时,即停止滴定.

(3)若滴定开始和结束时,酸式滴定管中的液面如图所示:已知用c(HCl)=0.10 mol/L的盐酸标定25mL的氢氧化钠溶液,测得c(NaOH)______ ___mol/L
(4)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是___ ___(填序号).
A.锥形瓶用蒸馏水洗净后没有干燥
B.碱式滴定管未用待测液润洗就直接注入待测氢氧化钠溶液
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体内有20多种微量元素,它们的质量总和不到体重的千分之一,但是对人体的健康却起着重要作用。下列各组元素全部是微量元素的是( )
A. Na、K、Cl、S、O
B. Mn、I、Fe、Zn、Cu
C. N、H、O、P、C
D. Mo、Ca、Cu、Mg、C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是( )
A.氯气通入水中,溶液呈酸性:Cl2+H2O ![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
B.用铜做电极电解CuSO4溶液:2Cu2++2H2O![]() 2Cu +O2↑+4H+
2Cu +O2↑+4H+
C.NaHS电离方程式:NaHS ![]() Na++HS-
Na++HS-
D.NH4Cl水解反应:NH4+ +2H2O ![]() NH3·H2O+H3O+
NH3·H2O+H3O+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:lg C(s)燃烧生成一氧化碳放出9.2kJ的热量;氧化亚铜与氧气反应的能量变化如图所示。下列叙述正确的是

A. 碳[C(s)]的燃烧热△H为-110.4kJ·mol-1
B. 1mol CuO分解生成Cu2O放出73kJ的热量
C. 反应2Cu2O(s)+O2(g)=4CuO(s)的△H为292 kJ·mol-1
D. 足量炭粉与CuO反应生成Cu2O的热化学方程式为:C(s)+2CuO(s)=Cu2O(s) +CO(g) △H=35.6kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com