
以下几种实验设计正确且能达到实验目的的有

A.1种 B.2种
C.3种 D.4种
科目:高中化学 来源: 题型:
一定量的NaHCO3和Na2CO3混合物,向其中加入500 mL HCl溶液后溶液呈中性,产生标况下CO2气体4.48 L,若将等量的NaHCO3和Na2CO3混合物加热后,产生气体(包括H2O)用碱石灰吸收,碱石灰增重4.65 g,则下列叙述正确的是
A.加热时生成的气体在标况下3.36 L
B.NaHCO3和Na2CO3混合物质量为17.9 g
C.加热时若用浓硫酸吸收气体则浓硫酸增重3.3 g
D.HCl溶液的浓度为0.6 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
咖啡鞣酸具有较广泛的抗菌作用,其结构简式如下图所示:

关于咖啡鞣酸的下列叙述正确的是 ( )
A.分子式为C16H13O9
B.1 mol咖啡鞣酸可与含8 mol NaOH的溶液反应
C.能使酸性KMnO4溶液褪色,说明分子结构中含有碳碳双键
D.与浓溴水能发生两种类型的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组设计用含氯的有机物A合成棉织物免烫抗皱整理剂M的路线如下(部分反应试剂和条件未注明):

已知:① E的分子式为C5H8O4,能发生水解反应,核磁共振氢谱显示E分子内有2种不同环境的氢原子,其个数比为3:1。
② 
(R、R′、R″代表相同或不相同的烃基)。
(1)A分子中的含氧官能团的名称是 。
(2)D→E反应的化学方程式是 。
(3)A→B反应所需的试剂是 。
(4)已知1 mol E 与2 mol J 反应生成1 mol M,则M的结构简式是 。
(5)E的同分异构体有下列性质:①能与NaHCO3反应生成CO2;②能发生水解反应,且水解产物之一能发生银镜反应,则该同分异构体共有 种,其中任意一种的结构简式是
(6)J 可合成高分子化合物,该高分子化合物结构简式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
1.下列相关家庭实验设计能达到预期目的的是
| 相关实验 | 预期目的 | |
| A | 在少量食用碱中滴加食醋 | 探究食用碱是碳酸钠还是碳酸氢钠 |
| B | 在食用盐中滴加少量淀粉液 | 探究食用盐是否为加碘盐 |
| C | 用激光笔照射淀粉液 | 探究淀粉液是胶体还是溶液 |
| D | 将鸡蛋白溶于水后,滴加AgNO3溶液 | 验证蛋白质中含有氯元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组探究SO2气体还原Fe3+,他们使用的药品和装置如图所示:
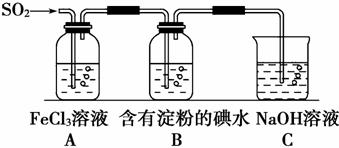
下列说法不合理的是
A.能表明I-的还原性弱于SO2的现象是B中蓝色溶液褪色
B.装置C的作用是吸收SO2尾气,防止污染空气
C.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2,产生白色沉淀
D.为了验证A中发生了氧化还原反应,加入KMnO4溶液,紫红色褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
把Ca(OH)2放入蒸馏水中,一段时间后达到平衡:
Ca(OH)2(s) Ca2+(aq)+2OH-(aq)。下列说法正确的是( )
Ca2+(aq)+2OH-(aq)。下列说法正确的是( )
A.恒温下向溶液中加入CaO,溶液的pH升高
B.给溶液加热,溶液的pH升高
C.向溶液中加入Na2CO3溶液,其中固体质量增加
D.向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如下:
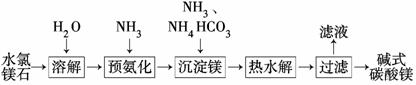
(1)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的Ksp=1.8×10-11,若溶液中c(OH-)=3.0×10-6 mol/L,则溶液中c(Mg2+)=_____ ___。
___。
(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为________。
(3)高温煅烧碱式碳酸镁得到MgO。取碱式碳酸镁4.66 g,高温煅烧至恒重,得到固体2.00 g和标准状况下CO2 0.896 L,通过计算确定碱式碳酸镁的化学式。
(4)若热水解不完全,所得碱式碳酸镁中将混有MgCO3,则产品中镁的质量分数________(填“升高”、“降低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于乙醇结构方面的说法中正确的是( )
A.乙醇结构中有-OH,所以乙醇溶解于水,可以电离出OH-而显碱性
B.乙醇与乙酸反应生成乙酸乙酯,所以乙醇显碱性
C.乙醇与钠反应可以产生氢气,所以乙醇显酸性
D.乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com