
下列叙述中正确的是( )
A.锅炉中沉积的CaSO4可用Na2CO3溶液浸泡后,再将不溶物用酸溶解去除
B.向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进了Fe3+水解
C.向纯水中加入盐酸或降温都能使水的离子积减小,电离平衡逆向移动
D.反应2A(g) + B(g)=3C (s) + D(g)在一定条件下能自发进行,说明该反应的ΔH>0
 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
某学生利用以下装置探究喷泉实验。其中A、F分别为硫化氢和氯气的发生装置,C为纯净干燥的氯气与硫化氢反应的装置。
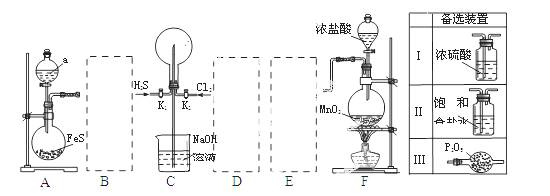
请回答下列问题:
(1)装置F中发生反应的化学方程式 。
(2)装置A中的分液漏斗内液体a可选用 (选填以下选项的代号)
A.盐酸 B.浓硫酸 C.稀硫酸 D.稀硝酸
(3)虚线框内应添加必要的除杂装置,请从上图的“备选装置”中选择合适装置的编号,填入下列空格。B__________、D__________、E__________。
(4)打开K1、K2,将常温压下的H2S、Cl2以体积比1:1充满烧瓶后,烧瓶中发生的反应用化学方程式表示为 ;关闭K1、K2,始终看不到烧瓶内产生“喷泉”现象,理由是: 。
(5)在操作(4)的基础上,引发喷泉操作方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学用语是表示物质组成、结构和变化规律的一种具有国际性、科学性和规范性的书面语言。下列化学用语中,书写错误的是( )
A.硫离子的结构示意图: B.NH4Cl的电子式:
B.NH4Cl的电子式: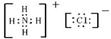
C.CO2的电子式: ············ D.次氯酸的结构式: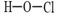
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度时,在2L容器中X、Y、Z三种气体随时间的变化关系曲线如图所示。
(1)由图中的数据分析,该反应的化学反应方程式为 ;
(2)反应开始至2min Z的平均反应速率为 ;
(3)若不改变外界条件,1min ~ 4min Z的生成速率(V1)与Z的反应速率(V2)的大小关系为:V1 V2(填 >、“< ”或“=”)。
”或“=”)。

查看答案和解析>>
科目:高中化学 来源: 题型:
人体血液里存在重要的酸碱平衡: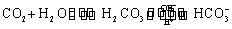 使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随
使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随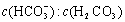 变化关系如下表:
变化关系如下表:
|
| 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.4 | 7.45 |
下列说法不正确的是( )
A.正常人体血液中,HCO3-的水解程度大于电离程度
B.人体血液酸中毒时,可注射NaHCO3溶液缓解
C.pH=7.00的血液中,c(H2CO3)<c(HCO3-)
D.pH=7.40的血液中,HCO3-的水解程度一定大于H2CO3的电离程度
查看答案和解析>>
科目:高中化学 来源: 题型:
2013年入冬以来,我国北方大部分地区连续出现雾霾天气。PM2.5是雾霾天气的主要
元凶,PM2.5是指大气中直径小于或等于2.5微米的颗粒物,它主要来自化石燃料的燃烧。下列相关说法正确的是( )
A.大力发展植树造林可从源头上减少雾霾天气的发生
B.由PM2.5形成的分散系属于胶体,具备胶体的性质
C.加快发展以氢燃料电池为能源的电动车,减少燃油车的使用
D.雾霾是由大量燃烧煤、天然气、石油等产生的CO2偏高所致
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A、水的离子积KW只与温度有关,但外加酸、碱、盐一定会影响水的电离程度
B、Ksp不仅与难溶电解质的性质和温度有关,还与溶液中相关离子的浓度有关
C、常温下,在0.10 mol·L-1的NH3·H2O溶液中加入少量NH4C1晶体,能使溶液的pH减小,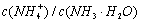 的比值增大
的比值增大
D、室温下,CH3COOH的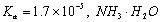 的
的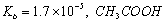 溶液中的c (H+)与NH3·H2O中的c(OH-)相等
溶液中的c (H+)与NH3·H2O中的c(OH-)相等
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有机物分子中,可形成顺反异构的是( )
A. CH2=CHCH3 B.CH2=CHCH2CH3 C.CH3CH=C(CH3)2 D.CH3CH=CHCl
查看答案和解析>>
科目:高中化学 来源: 题型:
氨是最重要的氮肥,是产量最大的化工产品之一。德国人哈伯在1905年发明了合成氨的方法,其合成原理为:N2(g)+3H2(g)  2NH3(g) ΔH= -92.4 kJ·mol-1,他因此获得了1918年诺贝尔化学奖。在密闭容器中,使2 mol N2和6 mol H2混合发生上述反应,达到平衡:
2NH3(g) ΔH= -92.4 kJ·mol-1,他因此获得了1918年诺贝尔化学奖。在密闭容器中,使2 mol N2和6 mol H2混合发生上述反应,达到平衡:
(1)此时,N2和H2的浓度比是 ;N2和H2的转化率比是 。
(2)若恒容下升高温度,则混合气体的相对分子质量 ;
密度 。(填“变大”“变小”或“不变”)。
(3)若充入氩气,并保持压强不变,平衡将 ;(填“正向”“逆向”或“不”)移动。
(4)若容器恒容、绝热, 加热使容器内温度迅速升至原来的2倍,达到新平衡后,
容器内温度 (填“大于”“小于”或“等于”)原来的2倍。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com