
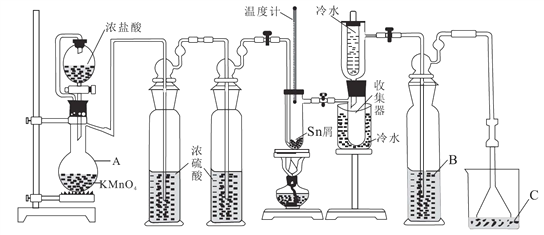
【题目】无水四氯化锡(SnCl4)常用作有机合成的氯化催化剂。实验室可用熔融的锡(熔点231.9℃)与Cl2反应制备SnCl4,装置如图所示。回答下列问题:
已知:①SnCl4在空气中极易水解生成SnO2·хH2O
②
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
SnCl2 | 无色晶体 | 246 | 652 |
SnCl4 | 无色液体 | -33 | 114 |
(1)仪器A的名称是_______,其中发生反应的离子方程式是____________。
(2)点燃酒精灯前需排尽装置中的空气,否则会发生副反应,化学方程式是______、_____。
(3)试剂 B、C依次为_______,试剂B的作用是______。
(4)Cl2 和锡的反应产物有SnCl4和SnCl2,为防止产品中带入 SnCl2,可采取的措施是_______、_______。
(5)碘氧化法滴定分析产品中2价Sn(II)的含量。准确称取m g产品于锥形瓶中,用蒸馏水溶解,淀粉-KI溶液做指示剂,用c mol·L-1 碘标准溶液滴定至终点,消耗碘标准溶液V mL,计算产品中Sn(II)的含量_______(用含c、m、V的代数式表示)。
【答案】 蒸馏烧瓶 2MnO4-+16H++10C1-=2Mn2++5C12↑+8H2O SnCl4 +(x+2)H2O=SnO2·xH2O↓+ 4 HCl↑ Sn+O2![]() SnO2 浓硫酸 氢氧化钠溶液 防止C溶液的水进入收集器 控制Sn与氯气的反应温度在232℃至650℃之间 过量氯气 (11.9cV/m)%
SnO2 浓硫酸 氢氧化钠溶液 防止C溶液的水进入收集器 控制Sn与氯气的反应温度在232℃至650℃之间 过量氯气 (11.9cV/m)%
【解析】(1)仪器A的名称是蒸馏烧瓶,其中浓盐酸和高锰酸钾反应生成氯化锰、氯气和水,发生反应的离子方程式是:2MnO4-+16H++10C1-=2Mn2++5C12↑+8H2O;(2)点燃酒精灯前需排尽装置中的空气,否则SnCl4在空气中极易水解生成SnO2·хH2O,发生的副反应是SnCl4+(x+2)H2O=SnO2·xH2O↓+4HCl↑,防止Sn 在加热时被空气中氧气氧化,发生的副反应为:Sn+O2![]() SnO2;(3)SnCl4在湿空气中极易水解生成SnO2·xH2O,通过试剂B防止水蒸气进入收集器,故试剂B为浓硫酸;氯气有毒,试剂C吸收氯气的余气,故试剂C为氢氧化钠溶液;试剂B的作用是防止C溶液的水进入收集器;(4)Cl2 和锡的反应产物有SnCl4和SnCl2,为防止产品中带入 SnCl2,可采取的措施是控制Sn与氯气的反应温度在232℃至650℃之间,SnCl4蒸出而SnCl2残留;以及用过量氯气,使产物SnCl4的比例增大;(5)根据反应I2+Sn2+=2I-+Sn4+可知,SnCl4的含量为
SnO2;(3)SnCl4在湿空气中极易水解生成SnO2·xH2O,通过试剂B防止水蒸气进入收集器,故试剂B为浓硫酸;氯气有毒,试剂C吸收氯气的余气,故试剂C为氢氧化钠溶液;试剂B的作用是防止C溶液的水进入收集器;(4)Cl2 和锡的反应产物有SnCl4和SnCl2,为防止产品中带入 SnCl2,可采取的措施是控制Sn与氯气的反应温度在232℃至650℃之间,SnCl4蒸出而SnCl2残留;以及用过量氯气,使产物SnCl4的比例增大;(5)根据反应I2+Sn2+=2I-+Sn4+可知,SnCl4的含量为![]() ×100%=
×100%=![]() 。
。


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究 , 其结构简式如图。下列关于分枝酸的叙述正确的是( )

A. 分子中含有2种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1 mol分枝酸最多可与3 mol NaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)乙酸乙酯用途广泛,在食品中可作为香料原料,现利用如下方法制备和提纯。
Ⅰ、制备
在试管a中先加入3mLCH3CH2OH,边摇动边缓缓加入2mL浓H2SO4并充分摇匀,冷却后再加入2mLCH3CO18OH,充分混合后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液。连接好装置。用酒精灯对试管a加热,当观察到试管b中有明显现象时停止加热。

(1)该装置有一处错误,请指出__________________________。
(2)试管a中生成乙酸乙酯的化学方程式(标记出18O的位置)______________________________。
(3)加入浓H2SO4的作用是______________________________。
II、提纯:

(1)操作1需用到_____________(填仪器名称),上层液体从该仪器的_________分离出来(填“上口”或“下口”)。
(2)请根据乙酸乙酯的性质选择合适的干燥剂__________。
a.氯化钙 b.碱石灰 c.硫酸铜
(3)试管b中混合液体在振荡过程中有气泡产生,该反应的化学方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子构型为正四面体的是( )
①P4 ②NH3 ③CCl4 ④CH4 ⑤H2S ⑥CO2
A.①③④⑤ B.①③④⑤⑥ C.①③④ D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焰火让国庆70周年联欢会更加辉煌壮观,这些五彩缤纷的焰火与元素的焰色反应有关。下列说法不正确的是
A.观察K2SO4的焰色应透过蓝色的钴玻璃
B.Na与NaCl在灼烧时火焰颜色相同
C.可以用焰色反应来区别NaCl和KCl
D.焰色反应一定发生化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2的燃烧热为285.8 kJ/mol,CO的燃烧热为282.8 kJ/mol。现有H2和CO组成的混合气体56.0 L(标准状况下),经充分燃烧后,一共放出热量710.0 kJ,并生成液态水。下列说法正确的是( )
A. CO燃烧的热化学方程式为2CO(g)+O2(g)===2CO2(g) ΔH=+282.8 kJ/mol
B. H2燃烧的热化学方程式为2H2(g)+O2(g)===2H2O(g) ΔH=-571.6 kJ/mol
C. 燃烧前的混合气体中,H2的体积分数为40%
D. 混合气体燃烧后与足量的过氧化钠反应,电子转移总数为2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用VSEPR模型预测下列分子或离子的立体结构,其中不正确的是( )
A. NH4+为正四面体形
B. CS2为直线形
C. HCN为折线形(V形)
D. PCl3为三角锥形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下:
元素 | 相关信息 |
A | 基态原子的价电子排布式为nSnnPn |
B | 基态原子中的未成对电子数是同周期中最多的 |
C | 最外层电子数是电子层数的3倍 |
D | 简单离子是第三周期元素中离子半径最小的 |
E | 价电子层中的未成对电子数为4 |
请回答下列问题(用对应元素的元素符号作答):
(1)写出D元素基态原子的价电子排布式 , E2+价电子的轨道表示式。
(2)这5种元素中电负性最大的元素是(填元素符号),A、B、C三种元素的第一电离能由大到小的顺序为(填元素符号)
(3)B、C、D的简单离子的半径由大到小的顺序为(用离子符号表示)
(4)写出C的核外有18个电子的氢化物的电子式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应:C+CO2=2CO中,可使反应速率增大的措施是( )
①增大压强 ②升高温度 ③通入CO2 ④增加碳的量 ⑤降低压强.
A.①②③
B.②③④⑤
C.①②③④
D.②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com