
| A. | 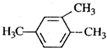 1,3,4-三甲基苯 1,3,4-三甲基苯 | B. | 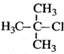 2-甲基-1-氯丙烷 2-甲基-1-氯丙烷 | ||
| C. | 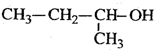 2-甲基-1-丙醇 2-甲基-1-丙醇 | D. | 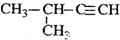 2-甲基-3-丁炔 2-甲基-3-丁炔 |
分析 A、选取最近的两个甲基,分别命名为1、2号碳;
B、选取含有氯原子的最长碳链,距离氯原子最近的一端为1号碳;
C、选取含有羟基的最长碳链为主链;
D、选取距离三键最近的一端为1号碳,据此解答即可.
解答 解:A、选取最近的两个甲基,分别命名为1、2号碳,正确命名应为:1,2,4-三甲基苯,故A错误;
B、选取含有氯原子的最长碳链,距离氯原子最近的一端为1号碳,正确命名为2-甲基-1-氯丙烷,故B正确;
C、选取含有羟基的最长碳链为主链,正确命名为:2-丁醇,故C错误;
D、选取距离三键最近的一端为1号碳,正确命名为:3-甲基-1-丁炔,故D错误,故选B.
点评 本题考查了苯的同系物命名、氯代烃的命名、炔烃以及醇类的命名,题目难度不大,注意习惯命名法和系统命名法对有机物的命名方法,该题注重了基础性试题的考查,侧重对学生基础知识的检验和训练.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:选择题
| A. | 若把H2S写成H3S,则违背了共价键的饱和性 | |
| B. | H3O+的存在说明共价键不应有饱和性 | |
| C. | 所有共价键都有方向性 | |
| D. | 两原子轨道发生重叠后,电子在两核间出现的概率减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
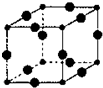 Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的巨大作用.
Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的巨大作用.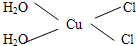 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 酸性:H2SO4>HClO4>HBrO4 | B. | 碱性:RbOH>KOH>NaOH | ||
| C. | 非金属性:P>S>Cl | D. | 气态氢化物稳定性:HF>HCl>H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑤⑦⑧ | B. | ①③④⑦⑨ | C. | ①⑤⑥⑧⑨ | D. | ①②③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
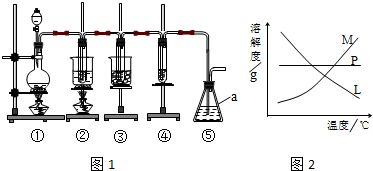
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为红色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成的HClO将石蕊氧化为无色物质 |
| 然后溶液从无色逐渐变为浅黄绿色色 | 继续通入的氯气溶于水使溶液呈浅黄绿色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO可以是某些含低价N物质氧化的产物 | |
| B. | NO难溶于水 | |
| C. | NO可以是某些含高价N物质还原的产物 | |
| D. | NO是红棕色气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com