
下列说法正确的是
A.其他条件不变时增大压强,能使全气体反应体系中活化分子百分数增加
B.中和反应都是放热反应
C.在FeCl3溶液和KSCN溶液反应的平衡体系中,加入KCl固体,平衡逆向移动
D.熵增大的反应不一定自发, 但自发反应熵一定增大
科目:高中化学 来源: 题型:
已知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,Ksp(Ag2CrO4)=2.0×10-12,则在相同温度下,下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是( )
A.AgCl>AgI>Ag2CrO4
B.AgCl> Ag2CrO4>AgI
Ag2CrO4>AgI
C.Ag2CrO4>AgCl>AgI
D.Ag2CrO4>AgI> AgCl
AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
聚乙炔导电聚合物的合成使高分子材料进入“合成金属”和塑料电子学时代,当聚乙炔分子带上药物、氨基酸、糖基等分子片后,就具有一定的生物活性。以下是我国化学家近年来合成的一些聚乙炔衍生物分子的结构简式:(Me指甲基)

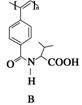
下列关于上述高分子的说法不正确的是( )
A.A和B均能在一定条件下水解,且水解形成相同的高分子
B.A中药物小分子羧酸的分子式为C16H18O4
C.B中氨基酸是一种α氨基酸
D.A和B各1 mol与热碱液反应,均最多消耗2n mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的说法不正确的是
A.测定中和热实验的玻璃仪器只需烧杯、量筒和温度计
B.用25mL碱式滴定管量取13.50mL Na2CO3溶液
C.用10mL量筒量取5.5mL硫酸溶液
D.用广泛pH试纸不能测得某碱溶液的pH为12.7
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于电化学原理应用中,正确的是
A.用惰性电极电解饱和食盐水时,阳极的电极反应式为:2H+-2e-=H2 ↑
B.氢氧燃料电池的负极反应式:O2 + 2H2O + 4e- == 4OH-
C.钢铁发生电化学腐蚀的负极反应式:Fe-2e- == Fe2+
D.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu -2e- == Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.常温下,如果取0.2mol/LHA溶液与0.2mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
(1) 混合溶液的pH=8的原因(用离子方程式表示):
__________________________________________。
(2) 混合溶液中由水电离出的c(H+)_____0.1mol/LNaOH溶液中由水电离出的c(H+)。(选填“大于”、“小于”或“等于”)
(3) 求出混合液中下列算式的精确计算结果(填具体数字):
c(Na+)-c(A-)=_________mol/L。
(4) 已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH__________7(选填“大于”、“小于”或“等于”);
Ⅱ.相同条件下,有pH均为4的盐酸、硫酸、醋酸三溶液,其物质的量浓度依次为
c1、c2、c3,则c1、c2、c3由大到小顺序为 。
Ⅲ.已知海水中镁离子浓度为1.8×10-3mol/L,且Ksp[Mg(OH)2] =1.8×10-11,常温下要使海水中镁离子产生沉淀,溶液的pH最低应为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
吗丁啉是一种常见的胃药,其有效成分的结构简式可用下图表示,关于该物质的下列说法不正确的是( )

A.该物质的分子式为C22H24ClN5O2
B.该物质具有碱性,能与酸反应
C.该物质不能发生水解反应
D.该物质能发生取代反应和加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com