
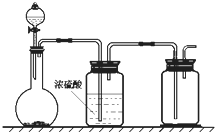
 如图装置,用于实验室发生、干燥和收集气体.(尾气处理装置已略去)能利用这套装置进行的实验是( )
如图装置,用于实验室发生、干燥和收集气体.(尾气处理装置已略去)能利用这套装置进行的实验是( )| A、电石与食盐水制C2H2 | B、块状大理石与稀硫酸制CO2 | C、铜屑和浓硝酸制NO2 | D、二氧化锰与浓盐酸制Cl2 |


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:阅读理解
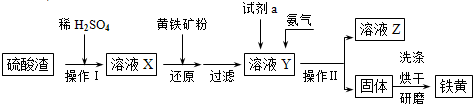
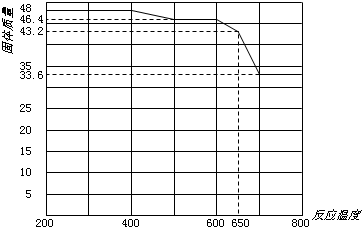
| H | + 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
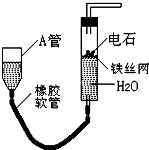 如图的实验装置可用于实验室中制取乙炔.请回答下列问题:
如图的实验装置可用于实验室中制取乙炔.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
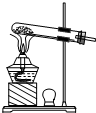
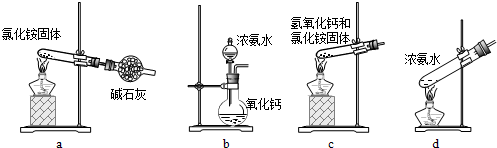
| A、除去碳酸钠固体中的碳酸氢钠杂质 | B、实验室用氯酸钾与二氧化锰制备氧气 | C、加热氯化铵与氢氧化钙固体混合物制取氨气 | D、实验室用二氧化锰与浓盐酸制氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
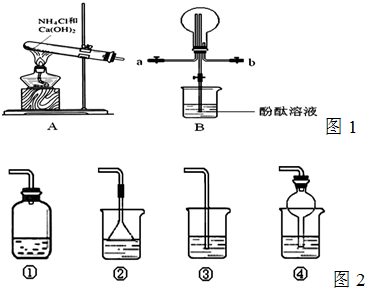
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com