

���� SnCl2���������ܽ⣬�ټ������ۣ��ܽ�õ�SnCl2��Һ����̼���Ƴ��������ӣ����˵õ�����ϴ�Ӻ���������ܽ�õ���������Һ������Ũ����ȴ�ᾧ������ϴ�ӵõ����������壬
��1����ԭ�ӵĺ˵����Ϊ50����̼Ԫ������ͬһ���壬���ڢ�A�壬����ԭ������������������Ԫ������ȷ�����ڵ����ڣ�
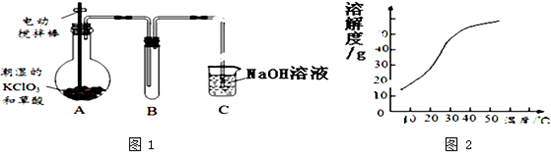
��2��������ͼ��֪���������Ǵ���Һ�еõ����ᾧˮ�ľ��壬ֻ�ܲ�ȡ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӵõ���
��3������Ϣ��֪��SnCl2��ˮ�����ɼ�ʽ�Ȼ��������������ᣬ����Sn2+ˮ�⣻
��4������Ϣ��֪��Sn2+�ױ�����������Sn�۳�������ҺpH�⣬����ֹSn2+��������
��5�����������£�SnSO4����������˫��ˮȥ������˫��ˮ��ǿ�����ԣ���Sn2+�ױ�����ΪSn4+����������ԭΪˮ��
��6�����ݵ���ת���غ��뷽��ʽ�ɵù�ϵʽSn��Sn2+��2Fe3+��2Fe2+��$\frac{1}{3}$K2Cr2O7���ݴ˼��㣮
��� �⣺SnCl2���������ܽ⣬�ټ������ۣ��ܽ�õ�SnCl2��Һ����̼���Ƴ��������ӣ����˵õ�����ϴ�Ӻ���������ܽ�õ���������Һ������Ũ����ȴ�ᾧ������ϴ�ӵõ����������壬
��1����Ԫ����̼Ԫ������ͬһ���壬���ڢ�A�壬ԭ�Ӻ˵����Ϊ50����50-2-8-8-18=14����Sn���ڵ������ڣ��������ڱ��е�λ��Ϊ�������ڵڢ�A�壬
�ʴ�Ϊ���������ڵڢ�A�壻
��2��������ͼ��֪���������Ǵ���Һ�еõ����ᾧˮ�ľ��壬ֻ�ܲ�ȡ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӵõ���
�ʴ�Ϊ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ�
��3������Ϣ��֪��SnCl2��ˮ�����ɼ�ʽ�Ȼ�����������ƽ��Sn Cl2+H2O?Sn��OH��Cl+HCl���������ᣬʹ��ƽ�������ƶ�������Sn2+ˮ�⣬
�ʴ�Ϊ��SnCl2ˮ�⣬����SnCl2+H2O?Sn��OH��Cl+HCl���������ᣬʹ��ƽ�������ƶ�������Sn2+ˮ�⣻
��4������Ϣ��֪��Sn2+�ױ�����������Sn�۳�������ҺpH�⣬����ֹSn2+��������
�ʴ�Ϊ����ֹSn2+��������
��5�����������£�SnSO4����������˫��ˮȥ������˫��ˮ��ǿ�����ԣ���Sn2+�ױ�����ΪSn4+����������ԭΪˮ�����ӷ���ʽΪ��Sn2++H2O2+2H+�TSn4++2H2O��
�ʴ�Ϊ��Sn2++H2O2+2H+�TSn4++2H2O��
��6����������������������Ϊx����
Sn��Sn2+��2Fe3+��2Fe2+��$\frac{1}{3}$K2Cr2O7���㣮
119g $\frac{1}{3}$mol
1.226g��x 0.100mol/L��0.032L
��$\frac{119g}{1.226xg}$=$\frac{\frac{1}{3}mol}{0.100mol/L��0.032L}$
���x=93.2%��
�ʴ�Ϊ��93.2%��
���� ����SnSO4�Ʊ���֮��Ϊ���壬����ѧ���Թ������̵����⡢���ʵķ����ᴿ���Ķ���Ŀ��ȡ��Ϣ�����������û�ѧ������д���ζ�Ӧ�ü����ù�ϵʽ���еļ���ȣ��Ѷ��еȣ���ѧ���Ļ���֪ʶ���������нϸߵ�Ҫ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
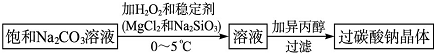
 �ߴ�MnCO3���Ʊ������ܴ��Բ��ϵ���Ҫԭ�ϣ�ʵ������MnO2Ϊԭ���Ʊ������ߴ�MnCO3�IJ����������£�
�ߴ�MnCO3���Ʊ������ܴ��Բ��ϵ���Ҫԭ�ϣ�ʵ������MnO2Ϊԭ���Ʊ������ߴ�MnCO3�IJ����������£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ�鲽�� | �����Լ� | ���ӷ���ʽ |
| ��1�� | ϡHCl | CO32-+2H+=CO2��+H2O |
| ��2�� | BaCl2��Һ | Ba2++SO42-=BaSO4�� |
| ��3�� | AgNO3��Һ | Ag++Cl-=AgCl�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ͼ��ʾ�������5minʱ��ͭ�缫��������2.16g���Իش�
��ͼ��ʾ�������5minʱ��ͭ�缫��������2.16g���Իش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �롡�� | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| Ũ��/mol•L-1 | 4��10-6 | 6��10-6 | 2��10-5 | 4��10-5 | 3��10-5 | 2��10-5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɫ��Һ�У�Al3+��Cl-��MnO4-��SO42- | |
| B�� | ���д���HCO3-����Һ�У�Na+��Ca2+��NO3-��Cl- | |
| C�� | 0.1mol•L-1AgNO3��Һ��H+��K+��SO42-��Cl- | |
| D�� | ʹʯ����ɫ����Һ��CH3COO-��Cl-��NO3-��K+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com