
将一定量的钠投入到12.3g t℃的水中,得到t℃时的氢氧化钠饱和溶液15.6g。试计算:
(1)该温度下氢氧化钠的溶解度是多少?
(2)反应掉的钠的质量是多少克?
科目:高中化学 来源: 题型:
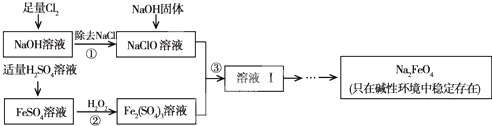
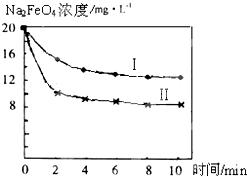
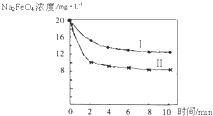 (2012?朝阳区一模)高铁酸钠(Na2FeO4)具有很强的氧化性,是一种新型的绿色净水消毒剂.工业上可以通过次氯酸钠氧化法制备高铁酸钠,生产过程如下:
(2012?朝阳区一模)高铁酸钠(Na2FeO4)具有很强的氧化性,是一种新型的绿色净水消毒剂.工业上可以通过次氯酸钠氧化法制备高铁酸钠,生产过程如下: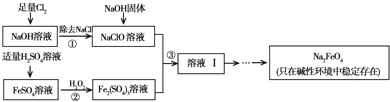
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:038
将一定量的钠投入到12.3gt℃的水中,得到t℃时的氢氧化钠饱和溶液15.6g.试计算:
(1)t℃时氢氧化钠的溶解度;
(2)反应掉的钠的质量.
查看答案和解析>>
科目:高中化学 来源: 题型:058
将一定量的钠投入到12.3gt℃的水中,得到t℃时的氢氧化钠饱和溶液15.6g.试计算:
(1)t℃时氢氧化钠的溶解度;
(2)反应掉的钠的质量.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com