
����Ŀ����������һ�����Լ�ǿ���������ᣬ�������Ʊ��������Ρ�������ʯ�ᴿ�ȷ��森�������ϵõ������йظ��������Ϣ��
���� | ����ʽ | ��� | �е� |
������ | HClO4 | ��ɫҺ�� | 130�� |
��ҵ�������������ͬʱ���������������ƣ���ҵ������ͼ��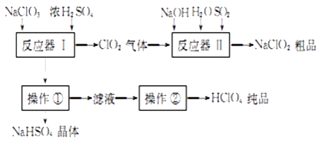
��1�������ٵ������� �� �����ڵ������� ��
��2����Ӧ�����з�����Ӧ�Ļ�ѧ����ʽΪ ��
��3����Ӧ�����з�����Ӧ�����ӷ���ʽΪ ��
��4������Ӧ������SO2��H2O2����Ҳ�ɴﵽͬ����Ŀ����ʱ������Ӧ�����ӷ���ʽΪ ��
��5������õ�201 kg�� HClO4��Ʒ��������ҪNaClO3 kg��
��6����ҵ��Ҳ���ò���������ͭ��������������Ƶø����ᣬ���������ɵõ�20%�ĸ����ᣮд�������ĵ缫��Ӧʽ������������������Ի�ѧʽ���֣� ��
���𰸡�
��1�����ˣ�����
��2��3NaClO3+3H2SO4=HClO4+2ClO2��+3NaHSO4+H2O
��3��4OH��+SO2+2ClO2=2ClO2��+SO42��+2H2O
��4��2ClO2+2OH��+H2O2=2ClO2��+O2+2H2O
��5��639
��6��HCl+4H2O��8e��=HClO4+8H+
���������⣺��1��ͨ�������ٵõ���Һ���������Ϊ���ˣ���ҺΪHClO4 �� ͨ�������ڵõ�������HClO4 �� �����֪��������ɽ�HClO4��ˮ�з���������Դ��ǣ����ˣ�����2��NaClO3��ŨH2SO4�ڷ�Ӧ��I�з�Ӧ��3NaClO3+3H2SO4=HClO4+2ClO2��+3NaHSO4+H2O��
���Դ��ǣ�3NaClO3+3H2SO4=HClO4+2ClO2��+3NaHSO4+H2O����3����Ӧ������ClO2����������������Ʒ�Ӧ�����������ƣ��䷴Ӧ�����ӷ���ʽΪ��4OH��+SO2+2ClO2=2ClO2��+SO42��+2H2O��
���Դ��ǣ�4OH��+SO2+2ClO2=2ClO2��+SO42��+2H2O����4������Ӧ������SO2��H2O2����Ҳ�ɴﵽͬ����Ŀ����ClO2��H2O2���������Ʒ�Ӧ�����������ƣ���H2O2������Ϊ���������ӷ���ʽΪ��2ClO2+2OH��+H2O2=2ClO2��+O2+2H2O��
���Դ��ǣ�2ClO2+2OH��+H2O2=2ClO2��+O2+2H2O����5������ҪNaClO3x��
���ݷ���ʽ
3NaClO3+3H2SO4= | HClO4+2ClO2��+3NaHSO4+H2O�� |
3��106.5g | 100.5g |
x | 201kg |
x=639kg��
���Դ��ǣ�639����6���������ĵ����У�������Cl��ʧ���ӷ���������Ӧ�Ĺ��̣����缫��ӦʽΪ��HCl+4H2O��8e��=HClO4+8H+��
���Դ��ǣ�HCl+4H2O��8e��=HClO4+8H+ ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��
P4�����ף�s��+5O2��g���TP4O10��s����H=��2983.2kJ/mol
P�����ף�s��+ ![]() O2��g���T
O2��g���T ![]() P4O10��s����H=��738.5kJ/mol
P4O10��s����H=��738.5kJ/mol
��д������ת��Ϊ�����Ȼ�ѧ����ʽ�������ȶ��ԱȺ�������ߡ��͡�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֤ʳƷ��ȫ������Ӫ�����⣬�DZ������彡���Ļ�����
�����������Ԫ�ش�ʳ������ȡ����ʱ����ͨ��ʳƷ���Ӽ��ͱ���ҩ���Բ��䣮���Ƴɲ��ơ���п�ı���ҩ�����Ƴɼӵ�ʳ�εȣ������Ӷ���ЩԪ�ص����������������ᵽ�IJ��Ƽ�����п���ͼӵ�ʳ���еĸơ�п������ָ����ѡ����ĸ����
A������ B��ԭ�� C��Ԫ�� D������
�ڱ�ù����Ⱦ����ʳ���������ù�أ�C17H12O6�����������������ڻ���ù�������»ᷢ��ͻ�䣬�̶��շ���֢������ù���������������л������
�����ڻ�ѧ����ʹ�ò���������ӡ�ѵĻ�ѧ����Խ��Խ�ࣺ�յ��졢�����谷������������������Σ�����彡������������ĸ����
A���ü�ȩ���ݺ��ʲ�Ʒ B����ù�仨��ѹեʳ����
C����С�մ����������ɼ� D���ù�ҵ������������������
��̼�������dz��õ����ɼ��������ڼ��������²������壬ʹʳƷ������ɣ���д����ط�Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijģ�⡰�˹���Ҷ���绯ѧʵ��װ����ͼ��ʾ����װ���ܽ�H2O��CO2ת��ΪO2��ȼ�ϣ�C3H8O��������˵����ȷ���ǣ� �� 
A.��װ�ý���ѧ��ת��Ϊ���ܺ͵���
B.��װ�ù���ʱ��H+��b������a����Ǩ��
C.ÿ����1 mol O2 �� ��44 g CO2����ԭ
D.a�缫�ķ�ӦΪ��3CO2+16H+��18e���TC3H8O+4H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鷽������У����е���
A. �ӹ���ϡ�������ˣ��ɳ�ȥ����ͭ���е�����þ�ۺ�����
B. ����ȡ�ķ����ɽ����ͺ�ú����з���
C. ���ܽ⡢���˵ķ����ɷ�������غ��Ȼ��ƹ�������
D. ����������������ͨ�����ȵ�����ͭ���Գ�ȥ���е�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״���һ����Ҫ�Ŀ�������Դ��
��1����֪��2CH4��g��+O2��g��=2CO��g��+4H2��g����H=a kJ/mol CO��g��+2H2��g��=CH3OH��g����H=b kJ/mol
д����CH4��O2��ȡCH3OH��g�����Ȼ�ѧ����ʽ�� ��
��2����Ӧ��CO��g��+2H2��g���TCH3OH��g����ƽ�ⳣ��K�ı���ʽΪ�� ͼ1�Ƿ�ӦʱCO��CH3OH��g�������ʵ���Ũ����ʱ�䣨t���ı仯���ߣ��ӷ�Ӧ��ʼ���ﵽƽ��ʱ����H2��ʾ�ķ�Ӧ����v��H2��= ��
��3����һ�ݻ��ɱ���ܱ������г���10mol CO��20mol H2 �� ������Ӧ���ﵽƽ�⣬CO��ƽ��ת�������¶ȣ�T����ѹǿ��P���ı仯������ͼ2��ʾ�� �����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������ѡ����ĸ����
A��H2���������ʵ���CH3OH���������ʵ�2��
B��H2������������ٸı�
C��H2��ת���ʺ�CO��ת�������
D����������ƽ����Է����������ٸı�
�ڱȽ�A��B����ѹǿ��С��P��A��P��B�������������������=������
�۱Ƚ�KA��KB��KC�Ĵ�С��
��4���Լ״�Ϊȼ�ϣ�O2Ϊ��������KOH��ҺΪ�������Һ�����Ƴ�ȼ�ϵ�أ��缫����Ϊ���Ե缫������KOH��Һ������д��ȼ�ϵ�ظ����ĵ缫��Ӧʽ�� �� 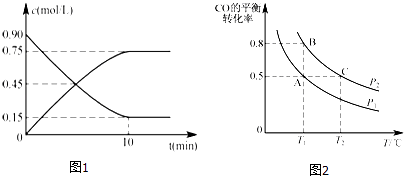
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͬѧͨ����ѯ����֪����һ��Ũ�ȵ�������Mg��Ӧʱ����ͬʱ�õ�NO2��NO��N2�������塣��ͬѧ��������������װװ����ֱ����֤��NO2��NO���ɲ���ȡ����þ (����ʵ����ÿ��ת��������ȫ��) ����������֪��
��NO2�е�Ϊ21.1 �桢�۵�Ϊ��11 �棬NO�е�Ϊ��151 �桢�۵�Ϊ��164 �棻
��þҲ����CO2��Ӧ��
�۵���þ��ˮ����ˮ������Mg(OH)2�Ͱ�����
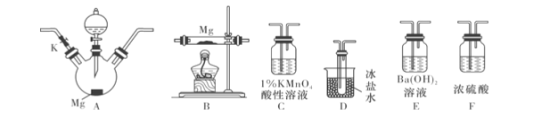
��1��Ϊʵ������ʵ��Ŀ�ģ���ѡ�õ���������ȷ���ӷ�ʽ�ǣ�A�� ��E��ʵ�����ȴ���K��ͨ��������װ����ͨ��CO2�������ų�װ���ڵĿ�����ֹͣͨ��CO2�ı�־�� ��
��2��ȷ����ԭ��������NO2�������� ��ʵ����Ҫ���ʹ��װ��F���ڶ���ʹ��F��Ŀ���� ��
��3��ʵ������У�������D�в���Ԥ�������ͬʱ��C����Һ��ɫ������ȥ����д��C�з�Ӧ�����ӷ���ʽ ��
��4����ͬѧ��A�п�ʼ��Ӧʱ�����ϵ�ȼB���ľƾ��ƣ�ʵ�������ͨ�����Է���B���IJ�Ʒ���Ȳ��ߣ�ԭ���� ��
��5�����һ��ʵ�鷽������֤þ�����ᷴӦʱȷʵ�а������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����Ʊ����״��ͱ�����Ļ�ѧԭ���ǣ�

��֪����ȩ�ױ��������������״��ķе�Ϊ205.3 �棬��������۵�Ϊ121.7 �棬�е�Ϊ249 �棬�ܽ��Ϊ0.34 g�����ѵķе�Ϊ34.8 �棬������ˮ���Ʊ����״��ͱ��������Ҫ����������ʾ��

�Ը���������Ϣ�ش��������⣺
(1)�������������________��������Һ�����ܽ����Ҫ�ɷ���________��
(2)�������������________����Ʒ����________��
(3)�������������________����Ʒ����________��

(4)��ͼ��ʾ�����������¶ȼ�ˮ�������ط��õ�λ��Ӧ��________(�a������b������c����d��)���ռ���Ʒ�������¶�Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2015��9��1�գ��Ĵ�������˸�����ӭ��118�����ա��п�ѧ�Ҷ������������м��������ĸ��״�л����������Ҷ�������������dz��ã��������ۣ�����Ѫ�ܼ����ļ���Ҳ�ܵͣ�����һ����й��ˣ�֬�ʴ�л���������縶���塣���ϲ��ϻش��������⣺
��1��֬����ϸ������Ҫ�Ļ�������У� �������֬�ʣ�Ҳ��ϸ�������õĴ������ʣ�����֮�⣬������ �� ��___________�Ĺ��ܡ������е� �ǹ���ϸ��Ĥ����Ҫ�ɷ֡�
��2����ʳ�й�������� ������Ѫ�ܱ����γɳ��������Ѫ�ܶ�����
��3��֬������ǡ������ʡ����ᶼ��ϸ������Ҫ���л���������к��������������ӣ����������� Ϊ�Ǽܣ����Ƕ����������������ɵ�λ���Ӷ��ɣ���Щ�����ĵ�λ��Ϊ���塣
��4����ɵ����ʵĵ���ķ��ӽṹͨʽ�ǣ� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com