
| A. | 四氯化碳的电子式: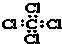 | B. | CH4分子的比例模型: | ||
| C. | 乙烯的球棍模型: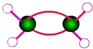 | D. | 乙炔的结构简式:CH≡CH |
分析 A.四氯化碳的电子式中,氯原子和碳原子的最外层都达到8电子稳定结构,氯离子漏掉了6个电子;
B.比例模型能够体现出原子的相对体积大小,甲烷分子为正四面体结构,分子中存在4个碳氢键;
C.球棍模型表现原子间的连接与空间结构;
D.乙炔含有碳碳三键,其官能团中必须标出官能团.
解答 解:A.四氯化碳为共价化合物,分子中存在4个碳氯共用电子对,氯原子最外层达到8电子稳定结构,四氯化碳正确的电子式为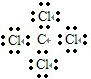 ,故A错误;
,故A错误;
B.甲烷分子中,碳原子的原子半径大于氢原子,甲烷中存在1个C、4个H,甲烷的比例模型为 ,故B正确;
,故B正确;
C.球棍模型表现原子间的连接与空间结构,乙烯的球棍模型: ,故C正确;
,故C正确;
D.乙炔的结构简式中需要标出碳碳三键,正确的结构简式为:CH≡CH,故D正确;
故选A.
点评 本题考查了电子式、比例模型、球棍模型、结构简式的判断,题目难度中等,注意掌握常见化学用语的概念及正确的表示方法,明确四氯化碳与甲烷的电子式的区别.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 已知H+(aq)+OH-(aq)═H2O(l);△H=-57.3kJ•mol-1,则H2SO4和Ba(OH)2反应的反应热△H=2×(-57.3)kJ•mol-1 | |
| B. | 燃料电池中将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g);△H=-192.9 kJ•mol-1,则CH3OH的燃烧热为192.9 kJ•mol-1 | |
| C. | H2(g)的燃烧热是285.8 kJ•mol-1,则2H2O(g)═2H2(g)+O2(g);△H=+571.6 kJ•mol-1 | |
| D. | 葡萄糖的燃烧热是2800 kJ•mol-1,则1/2 C6H12O6 (s)+3O2 (g)═3CO2 (g)+3H2O ( l );△H=-1400 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有① | B. | ①和③ | C. | ①和④ | D. | ②和③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8.5g | B. | 10.8g | C. | 6.2g | D. | 4.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④②③ | B. | ④③②① | C. | ②③④① | D. | ①④③② |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com