
| A. | 该装置将化学能转化为光能和电能 | |
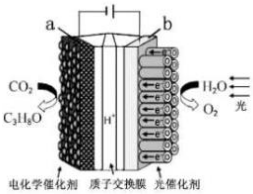
| B. | 该装置工作时,H+从a 极区向b 极区迁移 | |
| C. | 每有44 g CO2被还原,则生成标准状况下 33.6 L O2 | |
| D. | a 电极的反应为:3CO2+16H+-18e-═C3H8O+4H2O |
分析 A.根据图知,该装置有外接电源,属于电解池;
B.工作时,a是阴极、b是阳极,电解质溶液中阳离子向阴极移动、阴离子向阳极移动;
C.根据转移电子守恒计算生成氧气体积;
D.a电极上二氧化碳得电子和氢离子反应生成C3H8O、H2O.
解答 解:A.根据图知,该装置有外接电源,属于电解池,是将电能转化为化学能,故A错误;
B.工作时,a是阴极、b是阳极,电解质溶液中阳离子向阴极移动、阴离子向阳极移动,所以H+从b极区向a极区迁移,故B错误;
C.根据转移电子守恒计算生成氧气体积=$\frac{\frac{44g}{44g/mol}×6}{4}×22.4L/mol$=33.6L,故C正确;
D.a电极上二氧化碳得电子和氢离子反应生成C3H8O、H2O,电极反应式为3CO2+16H++18e-═C3H8O+4H2O,故D错误;
故选C.
点评 本题考查化学电源新型电池,为高频考点,明确各个电极上发生的反应、电解质溶液中离子移动方向等知识点是解本题关键,会根据转移电子守恒进行计算,难点是电极反应式的书写.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 电池工作时,电子由正极通过外电路流向负极 | |
| B. | 电池正极的电极反应式为:MnO2(s)+H2O(l)+e-═MnOOH(s)+OH-(aq) | |
| C. | 电池工作时,锌发生氧化反应 | |
| D. | 当电路中通过0.2mol电子,锌的质量理论上减小6.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
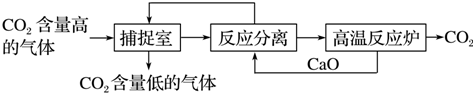
| A. | 生产过程中,可循环利用的物质有CaO和NaOH | |
| B. | 该方法涉及了化合、分解和复分解等反应类型 | |
| C. | 该方法通过化学变化,分离、提纯并利用CO2,可以减少碳的排放 | |
| D. | “反应分离”环节中,分离物质的基本操作是蒸发、结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2═CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH 加成反应 | |
| B. | 2CH3CH2OH $?_{140℃}^{浓硫酸}$CH3CH2OCH2CH3+H2O 消去反应 | |
| C. | 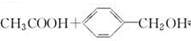 $?_{△}^{浓硫酸}$ $?_{△}^{浓硫酸}$ 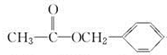 +H2O取代反应 +H2O取代反应 | |
| D. | 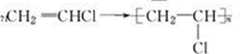 加聚反应 加聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O | |
| B. | 用FeCl3溶液腐蚀铜来制作印刷电路板:2Fe3++Cu═2Fe2++Cu2+ | |
| C. | 向Na2SiO3溶液中通入过量SO2:SiO32-+SO2+H2O═H2SiO3↓+SO32- | |
| D. | 向Al (SO4)3溶液中加入过量的NH3•H2O:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
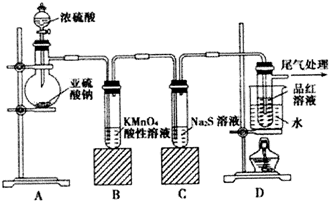
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用S制备H2SO4 | B. | 用CaCO3、Na2CO3、SiO2生产玻璃 | ||
| C. | 将海水中的MgSO4转变为金属Mg | D. | 用NO2生产HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向水中加入稀氨水,平衡逆向移动,c(OH-)降低 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 | |
| C. | 向水中加入少量固体NaOH,平衡逆向移动,c(H+)降低,KW减小 | |
| D. | 将水加热,KW增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 铝和氢氧化钠溶液共热 | |
| B. | 氯化铝溶液中滴入过量氢氧化钾溶液 | |
| C. | 明矾溶液中滴入过量氨水 | |
| D. | 物质的量浓度相同的硝酸铝溶液和氢氧化钠溶液等体积混合 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com