

| ||
| ||
| ||
| ||
| ||
| ||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、实验②证明了①的滤液中含有Ag+,由此推断①的滤液中也含有Cl? |
| B、实验②证明了该温度下Ag2S比Ag2SO4更难溶解 |
| C、实验③的溶液中含有Ag(NH3)2+微粒 |
| D、由实验③推测:若在①的沉淀中滴加NaOH溶液,沉淀也能溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某微粒空间构型为三角锥形,则该微粒一定是极性分子 |
| B、某微粒空间构型为V形,则中心原子一定有孤电子对 |
| C、sp3杂化轨道是由同一个原子中能量相近的s轨道和p轨道混合起来形成的一组新轨道 |
| D、凡是中心原子采取sp3杂化轨道成键的分子其立体构型都是正四面体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、按系统命名法,化合物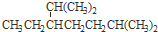 的名称为:2-甲基-5-丙基庚烷 的名称为:2-甲基-5-丙基庚烷 |
B、聚偏二氯乙烯( )的单体的结构简式为CCl2=CH2 )的单体的结构简式为CCl2=CH2 |
| C、有机物CH2=CH-CH=CH2和CH2=CH-CH3互为同系物 |
| D、李比希法、钠融法、铜丝燃烧法、元素分析仪均可帮助人们确定有机化合物的元素组成和空间结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| H2SO4 |
| NaOH |
| NaOH |
| H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①④⑤ | B、②③④ |
| C、①②④ | D、③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2Q2=Q1<Q |
| B、2Q2<Q1=Q |
| C、2Q2<Q1<Q |
| D、Q1=2Q2=Q |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com