
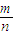 计算金属混合物的平衡相对原子质量,利用平均值法判断.
计算金属混合物的平衡相对原子质量,利用平均值法判断.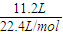 =0.5mol,
=0.5mol, ×27=18,Cu不反应,其的相对原子质量看做无穷大,平均值可能为24,故C正确;
×27=18,Cu不反应,其的相对原子质量看做无穷大,平均值可能为24,故C正确;

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:
 (2012?洛阳二模)如图所示,A、G、I均为单质,其中A、G为金属且都常被用作输电导线材料,B为黑色粉末,L是由两种元素组成的盐,它是家庭厨房必备物品.请回答:
(2012?洛阳二模)如图所示,A、G、I均为单质,其中A、G为金属且都常被用作输电导线材料,B为黑色粉末,L是由两种元素组成的盐,它是家庭厨房必备物品.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:



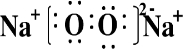
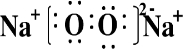
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 (2012?长宁区二模)短周期中常见金属X、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用).根据题意完成下列填空:
(2012?长宁区二模)短周期中常见金属X、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用).根据题意完成下列填空:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
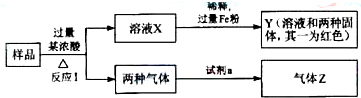
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:推断题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com