
【题目】下列反应中,水只作氧化剂的是①氟气通入水中 ②水蒸气经过灼热的焦炭 ③钠块投入水中④铁与水蒸气反应 ⑤氯气通入水中
A. 只有②③④ B. 只有①③⑤ C. 只有②③ D. 只有①④
【答案】A
【解析】
有电子转移的化学反应是氧化还原反应,其特征是反应前后有元素化合价的变化,在化学反应中得电子化合价降低的反应物是氧化剂,失电子化合价升高的反应物是还原剂;
①氟气通入水中2F2+2H2O=4HF+O2水只作还原剂;
②水蒸气经过灼热的焦炭,水只作氧化剂;
③钠块投入水中,2Na+2H2O=2NaOH+H2↑,水只作氧化剂;
④铁与水蒸气反应,3Fe+4H2O![]() Fe3O4+4H2,水只作氧化剂;
Fe3O4+4H2,水只作氧化剂;
⑤氯气通入水中Cl2+H2O=HCl+HClO,水中各元素的化合价都不变,所以水既不是氧化剂又不是还原剂。
根据以上水只作还原剂的反应①;水只作氧化剂②③④;水既不是氧化剂又不是还原剂⑤,故选A。


科目:高中化学 来源: 题型:
【题目】溶液X中可能含有K+、Mg2+、Al3+、AlO、SiO、CO、SO、SO中的若干种离子。某同学对该溶液进行了如下实验:

下列判断正确的是( )
A. 气体甲一定是纯净物 B. 沉淀甲是硅酸和硅酸镁的混合物
C. K+、AlO和SiO一定存在于溶液X中 D. CO和SO一定不存在于溶液X中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄酒常用Na2S2O5作抗氧化剂。中华人民共和国国家标准(G112760-2011)规定葡萄酒中抗氧化剂的残留量(以游离SO2计算)不能超过0.25g/L。某化学兴趣小组制备并对SO2的化学性质和用途进行探究,探究过程实验装置如下图,并收集某葡萄酒中SO2,对其含量进行测定。(夹持仪器省略)
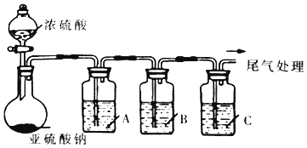
(1)实验可选用的实验试剂有浓硫酸、Na2SO3固体、Na2S溶液、BaCl2溶液、FeCl3溶液、品红溶液等.
①请完成下列表格
试剂 | 作用 | |
A | _____________ | 验证SO2的还原性 |
B | Na2S溶液 | _____________ |
C | 品红溶液 | ______________ |
②A中发生反应的离子方程式为______________________________________
(2)该小组收集某300.00mL葡萄酒中SO2,然后用0.0900 mol/L NaOH标准溶液进行滴定,滴定前排气泡时,应选择下图中的_________(填序号);若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处时,管内液体的体积_____(填序号)(①= 10mL;②=40mL; ③<10mL;④>40mL)

(3)该小组在实验室中先配制0.0900 mol/L NaOH标准溶液,然后再用其进行滴定。下列操作会导致测定结果偏高的是________。
A.未用NaOH标准溶液润洗滴定管
B.滴定前锥形瓶内有少量水
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D.配制溶液定容时,俯视刻度线
E.中和滴定时,观察标准液体积读数时,滴定前仰视,滴定后俯视
(4)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为_______g/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知自然界氧的同位素有16O、17O、18O,氢的同位素有H、D,从水分子的原子组成来看,自然界的水一共有( )
A. 3种 B. 6种 C. 9种 D. 12种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 对于同一个化学反应原子利用率和产率相同
B. 甲烷的三氯代物有两种结构
C. 石油的分馏是物理变化,煤的干馏是化学变化
D. 可以用裂化汽油萃取溴水中的溴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应 Zn(s) +H2SO4(aq)==ZnSO4(aq) +H2(g)的反应过程如下图所示, 下列叙述中不正确的是( )
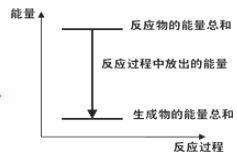
A. 若将该反应设计成原电池,正极可以是C 棒或 Fe 棒
B. 反应过程中滴加少量CuSO4 溶液可加快该反应的反应速率
C. H2SO4 的总能量大于ZnSO4 的总能量
D. 若将该反应设计成原电池,当有 32. 5g 锌溶解时,正极产生的气体在标的体积为 11. 2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2A(g)+3B(g)![]() 2C(g)+zD(g),现将2 mol A与2 mol B混合于2 L的密闭容器中,2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是
2C(g)+zD(g),现将2 mol A与2 mol B混合于2 L的密闭容器中,2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是
A. v(C)=0.2 mol·L-1·s-1 B. z=1
C. B的转化率为25% D. C平衡时的浓度为0.5mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常利用含硫废水生产Na2S2O3,原理是 S+Na2SO3![]() Na2S2O3 (Na2S2O3 稍过量,且该 反应的速率较慢;在酸性条件下,Na2S2O3 会自身发生氧化还原反应生成 SO2)。实验室可用如图装置(略 去部分夹持仪器)模拟生产过程。
Na2S2O3 (Na2S2O3 稍过量,且该 反应的速率较慢;在酸性条件下,Na2S2O3 会自身发生氧化还原反应生成 SO2)。实验室可用如图装置(略 去部分夹持仪器)模拟生产过程。
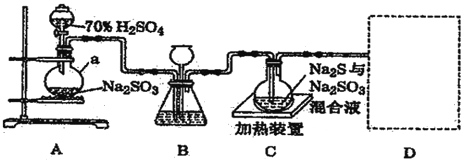
(1)Na2S2O3 中硫元素的化合价_______________。
(2)仪器 a 的名称______________,装置A中产生气体的化学方程式为_________________________ 。
(3)装置 B 的作用除观察 SO2 的生成速率外,长颈漏斗的作用是 ______________________________ 。
(4)装置 C 中需控制在碱性环境,否则产品发黄(生成黄色物质),用离子方程式表示其原因_________。
(5)装置 D 用于处理尾气,可选用的最合理装置(夹持仪器已略去)为___________(填字母)。
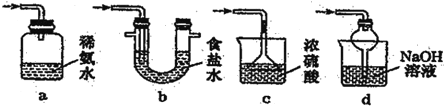
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知己烯(![]() )在常温下为液体,其分子结构中含有一个碳碳双键。下列有关物质的鉴别方法不可行的是( )
)在常温下为液体,其分子结构中含有一个碳碳双键。下列有关物质的鉴别方法不可行的是( )
A. 用酸性高锰酸钾溶液鉴别苯、己烯和己烷
B. 用燃烧法鉴别乙醇、苯和四氯化碳
C. 用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯
D. 用新制的![]() 悬浊液鉴别葡萄糖溶液、乙醇和乙酸
悬浊液鉴别葡萄糖溶液、乙醇和乙酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com