
����Ŀ��CH3COOOH���������ᣩ�㷺Ӧ���ڻ�����ҽԺ�����ҵ�������ijУ��ѧ��ȤС��������CH3COOH+H2O2=CH3COOOH+H2O����ȡ�������ᣬ�������������£�
���� | �е� �� | �۵� �� | �ܽ��� |
CH3COOH | 117.9 | 16.6 | ������ˮ���ƾ����л��ܼ� |
H2O2 | 150.2 | -0.43 | ����ˮ���ƾ� |
CH3COOOH | 105 | 0.1 | ����ˮ���ƾ����л��ܼ� |
ͬʱ��ù���������У��̼�����ζ����ȼ��������100�漴���ҷֽ⣻��������ȡ���������ը���Խ������н�ǿ�ĸ�ʴ�ԡ��ش��������⣺
��1��������ͼװ�ý�����ȡ��ʵ����ˮԡ�¶�Ӧ������________100�棨����>������<������=������ԭ���ǣ�____________________________________________________________
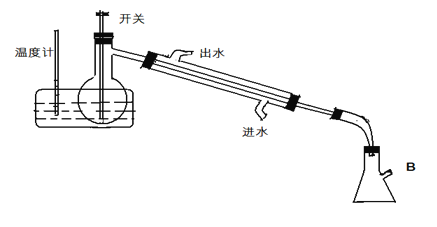
��2��Ϊ��ʹʵ��˳�����У�B��Ӧ��һ��_________����һ��װ�ã���Ȼ������ͼ�п���ͨ��������Ӷ��õ�����������Һ��
��3��ʵ�������õ�һ�����Ĺ������ᣬ�������·�Ӧ�ⶨ�ò���Ĵ��ȣ�
2KMnO4+5H2O2 +3H2SO4=K2SO4+2MnSO4+8H2O+5O2��
2KI+ CH3COOOH+2 H2SO4=2KHSO4+I2+ CH3COOH+H2O
I2+2Na2S2O3=2NaI+Na2S4O6
��ȡ10.00mL�ƵõĹ���������Һ����ˮϡ�͵�1000mL,����Һ��ȡ20.00mL����ƿ������������ϡ�����ữ��������____________��������ʽ�ζ�����������ʽ�ζ�������װ0.100mol/L��KMnO4��Һ���еζ���_______________________________________����ʱǡ����ȫ��Ӧ���Ӷ������ڹ��������е�H2O2��ȥ��Ȼ���ټ������KI��Һ�����뼸�ε��ۣ�����0.100mol/L��Na2S2O3�ζ�������12.00mL��һ�㹤ҵ�ƵõĹ���������������Ϊ18% ~ 23%��������ʵ�����ƵõĹ���������Һ�ܶ�Ϊ1.15gcm-3����ͨ�������жϸ���Һ�Ƿ�ϸ�_____________��
�ڵζ������У����в�����ʹ���ƫ�����_________��
A.�μ�Na2S2O3ʱ��ʼƽ�ӵζ��ܣ�����ʱ���ӵζ��ܡ�
B.װ��Na2S2O3��Һ�ĵζ���δ�ñ�Na2S2O3��Һ��ϴ��
C.��Һ����ʹ��֮ǰδ�ú�ɣ����渽��ˮ���������ȡ����Һ
D. .�μ�Na2S2O3ʱ��ʼ���ӵζ��ܣ�����ʱƽ�ӵζ��ܡ�
���𰸡� < CH3COOOH�ڸ���100��ʱ�����ҷֽ� ��ѹװ�� ��ʽ�ζ��� ���һ��ʱ����Һ�Ե���ɫ������30���ڲ���ȥ �����CH3COOOH����������Ϊ19.8%��Ϊ�ϸ� B
����������1��.������Ŀ��Ϣ��֪���������������100�漴���ҷֽ⣬�����¶�Ӧ����100�棬�ʴ��ǣ�<��CH3COOOH�ڸ���100��ʱ�����ҷֽ⣻
��2��.��������������100�������ҷֽ⣬����������ķе���105�棬����Ӧ��B����һ����ѹװ�ã��Է�ֹ��������ֽ⣬�ʴ�Ϊ����ѹװ�ã�
��3��. ��. ��KMnO4����ǿ�����ԣ�����Ӧ����ʽ�ζ���ʢװKMnO4��Һ�����������һ��ʱ����Һ�Ե���ɫ����30s�ڲ���ȥ��˵���ﵽ�˵ζ��յ㣻
��0.100mol/L��Na2S2O3�ζ�������Һʱ������12.00mL����n��Na2S2O3��=0.012L��0.100mol/L=0.0012mol����2KI+ CH3COOOH+2 H2SO4=2KHSO4+I2+ CH3COOH+H2O��I2 + 2Na2S2O3 = 2NaI + Na2S4O6 �ɵã�CH3COOOH��I2��2Na2S2O3����n��CH3COOOH��=1/2��n��Na2S2O3 ��=0.0006mol����ԭ10mL��Һ�к��й�����������ʵ���Ϊn��CH3COOOH��=0.0006mol��![]() =0.03mol��m��CH3COOOH��=0.03mol��76g/mol=2.28g��ԭ��Һ������Ϊ��10mL��1.15g/mL=11.5g��������������������Ϊ��
=0.03mol��m��CH3COOOH��=0.03mol��76g/mol=2.28g��ԭ��Һ������Ϊ��10mL��1.15g/mL=11.5g��������������������Ϊ�� ![]() ��100%=19.8%�����ϱ������Ը���Һ�ϸ����ʴ�Ϊ�� ��ʽ�ζ��������һ��ʱ����Һ�Ե���ɫ������30���ڲ���ȥ�������CH3COOOH����������Ϊ19.8%��Ϊ�ϸ�
��100%=19.8%�����ϱ������Ը���Һ�ϸ����ʴ�Ϊ�� ��ʽ�ζ��������һ��ʱ����Һ�Ե���ɫ������30���ڲ���ȥ�������CH3COOOH����������Ϊ19.8%��Ϊ�ϸ�
��. A.�μ�Na2S2O3ʱ��ʼƽ�ӵζ��ܣ�����ʱ���ӵζ�������ʹ�յ����ƫС�����Һ�����ƫС���ⶨ���ƫС����A������
B.װ��Na2S2O3��Һ�ĵζ���δ�ñ�Na2S2O3��Һ��ϴ����ʹ��Һ���ĵ����ƫ�ⶨ���ƫ��B��ȷ��
C.��Һ����ʹ��֮ǰδ��ɣ����渽��ˮ���������ȡ����Һ����ʹ��ȡ����Һ�����ƫС�����ı�Һ�����ƫС���ⶨ���ƫС����C����
D. .�μ�Na2S2O3ʱ��ʼ���ӵζ��ܣ�����ʱƽ�ӵζ�������ʹ��ʼ����ƫ�������Һ�����ƫС���ⶨ���ƫС����D������
�ʴ�ѡB��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ú������ҵ����ʳ����ʯ��������ҵ��ѪҺ�����й�ú��ʯ�ͼӹ���˵����ȷ����
A. ú�ĸ��������Ҫ�Ǹ����л���
B. ʯ�͵��ѽ⡢�����ú�ĸ������ڻ�ѧ�仯
C. ú���;�������ɵõ������ױ��ȣ�˵��ú�к��б��ͼױ�
D. ʯ�͵��ѻ���˵���������ڸ��������¿��Էֽ�Ϊ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���������;�������У�����ȷ����
A. ����������һ�����õİ뵼����� B. �������ƿ����ں������DZˮͧ�Ĺ�����
C. ��������������ҽ��θ���кͼ� D. ��������������ɫ�����Ϳ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڳ����л����˵������ȷ���ǣ� ��
A.�������֬������NaOH��Һ��Ӧ
B.����ϩ��ʹ��ˮ��ɫ
C.����ˮ������ά��ˮ��õ������ղ�����ͬ
D.�Ҵ�������������������ñ���Na2CO3��Һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������л�Ϊͬϵ����ǣ� ��
A.O2��O3
B.![]() C��
C�� ![]() C
C
C.CH4��CH3CH2CH3
D.CH3CH2CH2CH3�� ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС�����FeI2��Һ�л�õⵥ�ʣ������������ͼ��
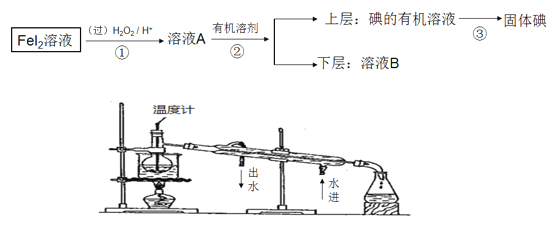
��ش�
��1���������г��ձ��⣬��Ҫ�õ��IJ���������������________________
��2����ͬѧ��ͼ����������ʵ�ֵڢ۲���������ͬѧ�������ͼ��ʵ��װ�ã���װ���е����Դ�����___________________________________
��3����ҺB�ʻ�ɫ�����˺�Fe3+�����ܻ�����I2���������һ��ʵ�鷽������֤�������ʵ�����������__________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1869�꣬������ѧ���Ž��з��������˵�һ��Ԫ�����ڱ�����Ϊ��ѧʷ�ϵ���Ҫ��̱�֮һ������˵���У�����ȷ����
A. Ԫ�����ڱ����߸�����
B. Ԫ�����ڱ���7�����壬7������
C. ��Ԫ��λ�ڵڶ����ڢ�A��
D. ϡ������Ԫ��ԭ�ӵ�������������Ϊ8��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͭ���仯�������ճ����������������Ź㷺��Ӧ�á��ش��������⣺
��1����Ԫ�������ڱ��е�λ����_______����̬Cu2+�ĺ�������Ų�ʽ��__________��Ԫ������ͭ�ĵڶ������ֱܷ�Ϊ��ICu=1958 kJ��mol-1��IFe=1561 kJ��mol-1��ICu��IFe��ԭ����_________________��
��2���л����������������غ���(��)����ѧʽΪ��[Fe(H2NCONH2)6](NO3)3��
�����ط�����Cԭ�ӵ��ӻ���ʽ��__________��
��[Fe(H2NCONH2)6](NO3)3 ����H2NCONH2���� Fe(��)֮�����������_______�����ݼ۲���ӶԻ��������Ʋ� NO3���Ŀռ乹��Ϊ____________��
��3��Fe3+����SCN�����飬���Ӧ���������֣��ֱ�Ϊ�����ᣨH-S-C��N�����������ᣨH-N=C=S�������������зе�ϸߵ���_______�� ԭ����______________��
��4��FeCl3����������ˮ���Ҵ����þƾ��Ƽ��ȼ����������ɴ˿�֪ FeCl3�ľ�������Ϊ______��S��Fe�γɵ�ij������侧����ͼһ��ʾ�� ������ʵĻ�ѧʽΪ__________��

��5��Cu����Ķѻ���ʽ��ͼ����ʾ��������Cuԭ�ӵ���λ��Ϊ_______����Cuԭ�Ӱ뾶Ϊa������ռ�������Ϊ _________���ú�a ��ʽ�ӱ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ȼ���У�����������̬��ʽ���ڣ������Ի���̬��ʽ���ڵ�Ԫ���ǣ� ��
A. �� B. �� C. �� D. ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com