
| A、18g D2O含有电子数为9NA |
| B、标准状况下,11.2L乙酸中含有的分子数目为0.5NA |
| C、78g Na2O2中含有的离子总数为4NA |
| D、1L 1mol?L-1 Na2CO3溶液中,溶液中CO32-离子数是NA |


 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
 |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 (25℃) |
Ka=1.8×10-5 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
| A、CN-+H2O+CO2=HCN+HCO3- |
| B、2CH3COOH+CO32-=2CH3COO-+H2O+CO2↑ |
| C、中和等体积、等pH的CH3COOH和HCN消耗NaOH的量前者小于后者 |
| D、等体积、等浓度的CH3COONa和NaCN溶液中所含离子总数前者小于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 检查气密性 |
B、 吸收HCl |
C、 制取Fe(OH)2沉淀 |
D、 稀释浓H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、两种气体的压强相等 |
| B、两种气体的氮原子数目不相等 |
| C、两种气体的分子数目相等 |
| D、NO比NO2的质量小 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、电解过程中N电极表面先有红色物质生成,后有气泡产生 |
| B、A点所得溶液只需加入一定量的CuO固体就可恢复到起始状态 |
| C、Q点时M、N两电极上产生的气体在相同条件下体积相同 |
| D、若M电极材料换成Cu做电极,则电解过程中CuSO4溶液的浓度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等物质的量的 CO2与氢氧化钠溶液反应:CO2+OH-=HCO3- | ||||
| B、少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | ||||
| C、Ca(OH)2溶液与等物质的量的稀H2SO4混合:Ca2++2OH-+2H++SO42-═CaSO4↓+2H2O | ||||
D、用石墨电极电解饱和食盐水:2H2O+2Cl-
|
查看答案和解析>>
科目:高中化学 来源: 题型:
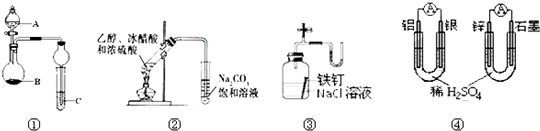
| A、图①中,若A为浓盐酸,B为MnO2,C中盛石蕊试液,则C中溶液先变红后褪色 |
| B、图②制备乙酸乙酯 |
| C、图③证明铁生锈与空气有关 |
| D、图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com