
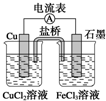
 ��ͼ��ʾΪijԭ��صĽṹʾ��ͼ������˵������ȷ���ǣ�������װ���ñ���KCl��Һ���������ɵĶ�������������
��ͼ��ʾΪijԭ��صĽṹʾ��ͼ������˵������ȷ���ǣ�������װ���ñ���KCl��Һ���������ɵĶ�������������| A����ԭ��ص��ܷ�ӦʽΪ2Fe3++Cu�T2Fe2++Cu2+ |
| B���õ�ع���ʱ��Cu2+�ڵ缫�ϵõ����ӣ�������ԭ��Ӧ |
| C�����ô˵�ص�ⱥ���Ȼ�����Һ��ȡCl2����ͭ�缫����������6.4 gʱ���������������Ϊ2.24 L������Ϊ��״���� |
| D����ع��������У�������ͭ�缫��������������ʯī�缫 |


 �Ƹ�С״Ԫ�������������ϵ�д�
�Ƹ�С״Ԫ�������������ϵ�д� ����һ������ܼƻ�ϵ�д�
����һ������ܼƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ҩ�ǰѲݵijɷ�֮һM��������ɱ�����ã�M�Ľṹ��ͼ��ʾ����������ȷ���ǣ�������
��ҩ�ǰѲݵijɷ�֮һM��������ɱ�����ã�M�Ľṹ��ͼ��ʾ����������ȷ���ǣ�������| A��M����Է���������178 |
| B��1mol M�������2mol Br2������Ӧ |
| C��M��������NaOH��Һ������Ӧʱ�������л�����Ļ�ѧʽΪC9H4O5Na4 |
| D��1mol M������NaHCO3��Ӧ������2mol CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����0.1mol?L-1�Ĵ�����ҺpH=a������ϡ��10������Һ��pH=b����a��b |
| B���ڵ��з�̪��Һ�İ�ˮ�����NH4Cl����Һǡ����ɫ�����ʱ��Һ��pH��7 |
| C��1.0��10-3mol/L�����pH=3��1.0��10-8mol/L�����pH=8 |
| D����1mL pH=1��������100 mL NaOH��Һ��Ϻ���Һ��pH=7��NaOH��Һ��pH=11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2mol | B��3mol |
| C��4mol | D��6mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����С�����һСʱ��Ϩ�ƻ |
| B������̫�������� |
| C���������صġ�������ʳ�� |
| D�����������������ۣ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢� | B���ڢ� | C���٢� | D���ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������ | NH4+��Na+��Mg2+ |
| ������ | OH-��NO3-��SO42- |
| A������һ����Na+ |
| B������һ����NH4+ |
| C������һ����Mg2+ |
| D������һ����SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� |

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com