
| 实验装置 | 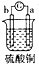 | 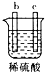 | 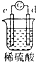 | 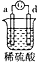 |
| 部分实验现象 | A极质量减小,b极质量增加 | B极有气体产生,c极无变化 | D极溶解,c极有气体产生 | 电流从a极流向d极 |
| A. | a>b>c>d | B. | b>c>d>a | C. | d>a>b>c | D. | a>b>d>c |
分析 根据 中发生化学腐蚀,活泼金属与酸反应放出氢气,不活泼金属与酸不反应;
中发生化学腐蚀,活泼金属与酸反应放出氢气,不活泼金属与酸不反应;
根据 、
、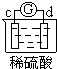 、
、 中发生电化学腐蚀,活泼金属作负极,不活泼金属作正极,负极发生氧化反应,正极发生还原反应,电子从负极经外电路流向正极,电流和电子分析相反,据此来回答判断.
中发生电化学腐蚀,活泼金属作负极,不活泼金属作正极,负极发生氧化反应,正极发生还原反应,电子从负极经外电路流向正极,电流和电子分析相反,据此来回答判断.
解答 解: 中发生化学腐蚀,b极有气体产生,c极无变化,所以金属的活动性顺序b>c;
中发生化学腐蚀,b极有气体产生,c极无变化,所以金属的活动性顺序b>c; 中发生电化学腐蚀,a极质量减小,b极质量增加,a极为负极,b极为正极,所以金属的活动性顺序a>b;
中发生电化学腐蚀,a极质量减小,b极质量增加,a极为负极,b极为正极,所以金属的活动性顺序a>b; 中发生电化学腐蚀,电流从a极流向d极,a极为正极,d极为负极,所以金属的活动性顺序d>a;
中发生电化学腐蚀,电流从a极流向d极,a极为正极,d极为负极,所以金属的活动性顺序d>a; 中发生电化学腐蚀,d极溶解,所以d是负极,c极有气体产生,所以c是正极,所以金属的活动性顺序d>c;
中发生电化学腐蚀,d极溶解,所以d是负极,c极有气体产生,所以c是正极,所以金属的活动性顺序d>c;
所以这四种金属的活动性顺序d>a>b>c,
故选C.
点评 本题主要考查了金属的活动性,掌握金属的腐蚀原理是解题的关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| B. | 二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 | |
| C. | 生石灰能与水反应,可用来干燥氯气 | |
| D. | 从海水中提取物质都必须通过化学反应才能实现 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A>B>C>D | B. | D>B>A>C | C. | B>A>C>D | D. | C>A>B>D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CH3)2CHCH2Br在碱性溶液中水解 | B. | 苯在常温下与Fe、液溴反应 | ||
| C. | 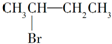 与NaOH的醇溶液共热反应 与NaOH的醇溶液共热反应 | D. | 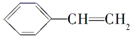 在催化剂存在下与H2完全加成 在催化剂存在下与H2完全加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
 ;⑪
;⑪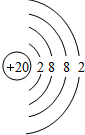 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用一定量NaOH稀溶液和稀盐酸反应测得的中和热数据,来推算一定量的稀H2SO4和NaOH稀溶液反应的反应热 | |
| B. | 用沸点数据推测能否用蒸馏的方法将两种液体混合物进行分离 | |
| C. | 用反应热数据的大小判断不同反应的反应速率大小 | |
| D. | 用原子(或离子)半径数据推断某些原子(或离子)氧化性或还原性的强弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com