
CO2ŗĶCH4ŹĒĮ½ÖÖÖŲŅŖµÄĪĀŹŅĘųĢ壬ĶعżCH4ŗĶCO2·“Ó¦ÖĘŌģøüøß¼ŪÖµ»ÆѧʷŹĒÄæĒ°µÄŃŠ¾æÄæ±ź”£
£Ø1£©250”ꏱ£¬ŅŌÄųŗĻ½šĪŖ“߻ƼĮ£¬Ļņ4 LČŻĘ÷ÖŠĶØČė6 mol CO2”¢6 mol CH4£¬·¢ÉśČēĻĀ·“Ó¦£ŗCO2 (g)£«CH4(g) 2CO(g)£«2H2(g)”£Ę½ŗāĢåĻµÖŠø÷×é·ÖĢå»ż·ÖŹżČēĻĀ±ķ£ŗ
2CO(g)£«2H2(g)”£Ę½ŗāĢåĻµÖŠø÷×é·ÖĢå»ż·ÖŹżČēĻĀ±ķ£ŗ
| ĪļÖŹ | CH4 | CO2 | CO | H2 |
| Ģå»ż·ÖŹż | 0.1 | 0.1 | 0.4 | 0.4 |
¢Ł“ĖĪĀ¶ČĻĀøĆ·“Ó¦µÄĘ½ŗā³£ŹżK=__________
¢ŚŅŃÖŖ£ŗCH4(g)£«2O2(g)£½CO2(g)£«2H2O(g) ”÷H=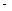 890.3 kJ·mol£1
890.3 kJ·mol£1
CO(g)£«H2O (g)£½CO2(g)£«H2 (g) ”÷H=+2.8 kJ·mol£1
2CO(g)£«O2(g)£½2CO2(g) ”÷H=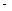 566.0 kJ·mol£1
566.0 kJ·mol£1
·“Ó¦CO2(g)£«CH4(g) 2CO(g)£«2H2(g) µÄ”÷H=________________
2CO(g)£«2H2(g) µÄ”÷H=________________
£Ø2£©ŅŌ¶žŃõ»ÆīѱķĆęø²øĒCu2Al2O4ĪŖ“߻ƼĮ£¬æÉŅŌ½«CO2ŗĶCH4Ö±½Ó×Ŗ»Æ³ÉŅŅĖį”£
¢ŁŌŚ²»Ķ¬ĪĀ¶ČĻĀ“߻ƼĮµÄ“߻Ɗ§ĀŹÓėŅŅĖįµÄÉś³ÉĖŁĀŹČēÓŅĶ¼ĖłŹ¾”£250”«300”ꏱ£¬ĪĀ¶ČÉżø߶ųŅŅĖįµÄÉś³ÉĖŁĀŹ½µµĶµÄŌŅņŹĒ_____________________

¢ŚĪŖĮĖĢįøßøĆ·“Ó¦ÖŠCH4µÄ×Ŗ»ÆĀŹ£¬æÉŅŌ²ÉČ”µÄ“ėŹ©ŹĒ________________________
¢Ū½«Cu2Al2O4ČܽāŌŚĻ”ĻõĖįÖŠµÄĄė×Ó·½³ĢŹ½ĪŖ___________________________
£Ø3£©Li2O”¢Na2O”¢MgO¾łÄÜĪüŹÕCO2”£¢ŁČē¹ūŃ°ÕŅĪüŹÕCO2µÄĘäĖūĪļÖŹ£¬ĻĀĮŠ½ØŅéŗĻĄķµÄŹĒ______
a.æÉŌŚ¼īŠŌŃõ»ÆĪļÖŠŃ°ÕŅ
b.æÉŌŚ¢ńA”¢¢ņA×åŌŖĖŲŠĪ³ÉµÄŃõ»ÆĪļÖŠŃ°ÕŅ
c.æÉŌŚ¾ßÓŠĒæŃõ»ÆŠŌµÄĪļÖŹÖŠŃ°ÕŅ
¢ŚLi2OĪüŹÕCO2ŗ󣬲śĪļÓĆÓŚŗĻ³ÉLi4SiO4£¬Li4SiO4ÓĆÓŚĪüŹÕ”¢ŹĶ·ÅCO2”£ŌĄķŹĒ£ŗŌŚ500”ę£¬CO2ÓėLi4SiO4½Ó“„ŗóÉś³ÉLi2CO3£»Ę½ŗāŗó¼ÓČČÖĮ700”ę£¬·“Ó¦ÄęĻņ½ųŠŠ£¬·Å³öCO2£¬Li4SiO4ŌŁÉś£¬ĖµĆ÷øĆŌĄķµÄ»Æѧ·½³ĢŹ½ŹĒ___________________________
£Ø4£©ĄūÓĆ·“Ó¦Aæɽ«ŹĶ·ÅµÄCO2×Ŗ»ÆĪŖ¾ßÓŠ¹¤ŅµĄūÓĆ¼ŪÖµµÄ²śĘ·”£
·“Ó¦A£ŗ
øßĪĀµē½ā¼¼ŹõÄÜøߊ§ŹµĻÖ£Ø3£©ÖŠ·“Ó¦A£¬¹¤×÷ŌĄķŹ¾ŅāĶ¼ČēĻĀ£ŗ
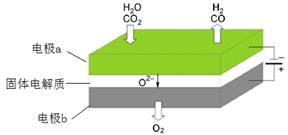
CO2ŌŚµē¼«a·ÅµēµÄ·“Ó¦Ź½ŹĒ_____________________________________________
”¾ÖŖŹ¶µć”æ·“Ó¦ČČµÄ¼ĘĖć”¢»ÆŃ§Ę½ŗā³£ŹżµÄŗ¬Ņ唢»ÆŃ§Ę½ŗāµÄÓ°ĻģŅņĖŲ”¢µē½āŌĄķ
”¾“š°ø½āĪö”æ¢Å¢Ł64 ¢Ś+247.3 kJ·mol£1
¢Ę¢ŁĪĀ¶Č³¬¹ż250”ꏱ£¬“߻ƼĮµÄ“߻Ɗ§ĀŹ½µµĶ
¢ŚŌö“ó·“Ó¦Ń¹Ēæ»ņŌö“óCO2µÄÅضČ
¢Ū3Cu2Al2O4+32H++2NO3£=6Cu2++ 6Al3++2NO”ü+16 H2O
£Ø3£©¢Łab £Ø1·Ö£© ¢ŚCO2 + Li4SiO4  Li2CO3 + Li2SiO3
Li2CO3 + Li2SiO3
£Ø4£©CO2 + 2e- == CO+O2-
½āĪö£ŗ£Ø1£©¢Ł CO2£Øg£©+CH4£Øg£©⇌2CO£Øg£©+2H2£Øg£©
ĘšŹ¼£Ømol£© 6 6 0 0
·“Ó¦£Ømol£© X X 2X 2X
Ę½ŗā£Ømol£© 6-X 6-X 2X 2X
ÓÉCH4µÄĢå»ż·ÖŹżĪŖ0.1£¬Ōņ(6-x)/(12+2x)=0.1£¬½āµĆX=4£¬ĖłŅŌK=(22”Į22)/(0.5”Į0.5)=64
¢ŚCH4£Øg£©+2O2£Øg£©=CO2£Øg£©+2H2O£Øg£©”÷H=-890.3kJ•mol-1 ¢Ł
CO£Øg£©+H2O £Øg£©=CO2£Øg£©+H2 £Øg£©”÷H=2.8kJ•mol-1 ¢Ś
2CO£Øg£©+O2£Øg£©=2CO2£Øg£©”÷H=-566.0kJ•mol-1 ¢Ū
øł¾ŻøĒĖ¹¶ØĀÉ£¬ÓÉ¢Ł+¢Ś”Į2-¢Ū”Į2µĆ
CO2£Øg£©+CH4£Øg£©⇌2CO£Øg£©+2H2£Øg£©”÷H=(-890.3+2.8”Į2+566.0”Į2) kJ•mol-1=+247.3 kJ•mol-1£»
£Ø2£©¢ŁĪĀ¶Č³¬¹ż250”ꏱ£¬“߻ƼĮµÄ“߻Ɗ§ĀŹ½µµĶ£¬ĖłŅŌĪĀ¶ČÉżø߶ųŅŅĖįµÄÉś³ÉĖŁĀŹ½µµĶ£»
¢ŚŌö“ó·“Ó¦Ń¹Ē攢Ōö“óCO2µÄÅØ¶Č£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬·“Ó¦Īļ×Ŗ»ÆĀŹŌö“ó£»
¢ŪCu2Al2O4²š³ÉŃõ»ÆĪļµÄŠĪŹ½£ŗCu2O•Al2O3£¬ÓėĖį·“Ӧɜ³ÉĄė×Ó·½³ĢŹ½£ŗ
3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO”ü+16H2O£»
£Ø3£©¢Ła£®Li2O”¢Na2O”¢MgO¾łŹōÓŚ¼īŠŌŃõ»ÆĪļ£¬¾łÄÜĪüŹÕĖįŠŌŃõ»ÆĪļCO2£¬æÉŌŚ¼īŠŌŃõ»ÆĪļÖŠŃ°ÕŅĪüŹÕCO2µÄĘäĖūĪļÖŹ£¬¹ŹaÕżČ·£»
b£®Li2O”¢Na2O”¢MgO¾łÄÜĪüŹÕCO2£¬ÄĘ”¢Ć¾”¢ĀĮĪŖ¢ńA”¢¢ņA×åŌŖĖŲ£¬ĖłŅŌæÉŌŚ¢ńA”¢¢ņA×åŌŖĖŲŠĪ³ÉµÄŃõ»ÆĪļÖŠŃ°ÕŅĪüŹÕCO2µÄĘäĖūĪļÖŹ£¬¹ŹbÕżČ·£»
c£®Li2O”¢Na2O”¢MgO¾łÄÜĪüŹÕCO2£¬µ«ĖüĆĒ¶¼Ć»ÓŠĒæŃõ»ÆŠŌ£¬ĒŅĪüŹÕ¶žŃõ»ÆĢ¼ÓėŃõ»Æ»¹ŌĪŽ¹Ų£¬¹Źc“ķĪó£» ¹Ź“š°øĪŖ£ŗab£»
¢ŚŌŚ500”ę£¬CO2ÓėLi4SiO4½Ó“„ŗóÉś³ÉLi2CO3£¬·“Ó¦ĪļĪŖCO2ÓėLi4SiO4£¬Éś³ÉĪļÓŠLi2CO3£¬øł¾ŻÖŹĮæŹŲŗćæÉÖŖ²śĪļ»¹ÓŠLi2SiO3£¬ĖłŅŌ»Æѧ·½³ĢŹ½ĪŖCO2 + Li4SiO4  Li2CO3 + Li2SiO3£»
Li2CO3 + Li2SiO3£»
£Ø4£©¶žŃõ»ÆĢ¼ŌŚa¼«µĆµ½µē×Ó·¢Éś»¹Ō·“Ӧɜ³ÉŅ»Ńõ»ÆĢ¼Ķ¬Ź±Éś³ÉŃõĄė×Ó£¬·“Ó¦µē¼«·“Ó¦Ź½ĪŖ£ŗCO2+2e-═CO+O2-£»
”¾Ė¼Ā·µć²¦”æ±¾ĢāÖ÷ŅŖæ¼²éĮĖ×ŪŗĻĄūÓĆCO2£¬Éę¼°ČČ»Æѧ·“Ó¦”¢µē»Æѧ”¢»ÆŃ§Ę½ŗāÓ°ĻģŅņĖŲµČ£¬½ĻĪŖ×ŪŗĻ£¬ĢāÄæÄѶČÖŠµČ


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ņ»¶ØĪĀ¶ČĻĀ£¬·“Ó¦2SO2 + O2  2SO3£¬“ļµ½Ę½ŗāŹ±£¬n(SO2):n(O2):n(SO3) £½ 2:3:4”£ĖõŠ”Ģå»ż£¬·“Ó¦ŌŁ“Ī“ļµ½Ę½ŗāŹ±£¬n(O2)£½0.8mol£¬n(SO3)£½1.4mol£¬“ĖŹ±SO2µÄĪļÖŹµÄĮæÓ¦ŹĒ
2SO3£¬“ļµ½Ę½ŗāŹ±£¬n(SO2):n(O2):n(SO3) £½ 2:3:4”£ĖõŠ”Ģå»ż£¬·“Ó¦ŌŁ“Ī“ļµ½Ę½ŗāŹ±£¬n(O2)£½0.8mol£¬n(SO3)£½1.4mol£¬“ĖŹ±SO2µÄĪļÖŹµÄĮæÓ¦ŹĒ
AӢ0.4mol BӢ0.6mol CӢ0.8mol DӢ1.2mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ¹ŲÓŚ»ÆѧÓĆÓļµÄ±ķŹ¾ÕżČ·µÄŹĒ
A£®Ć¾Ąė×Ó½į¹¹Ź¾ŅāĶ¼£ŗ 
B£®ÖŹ×ÓŹżÓėÖŠ×ÓŹżĻąµČµÄĮņŌ×Ó£ŗ S
S
C£®¶ž·ś»ÆŃõ·Ö×Óµē×ÓŹ½£ŗ 
D£®¶Ō¼×»ł±½·Ó½į¹¹¼ņŹ½£ŗ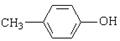
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½«”°·ĻŌÓĶŃĢ³¾”±ÓĆĮņĖįĪüŹÕ½žČ”£¬¼Čæɱ£»¤»·¾³ÓÖæɵƵ½ÓĆĶ¾¹ć·ŗµÄøß“æĮņĖįŠæ”£ŅŃÖŖŃĢ³¾ÖŠÖ÷ŅŖŗ¬ZnO£¬»¹ÓŠÉŁĮæµÄFeO”¢Fe2O3”¢CuO”¢MnO”£Öʱø¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ
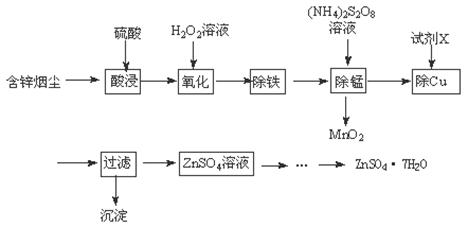
£Ø1£©ĮņĖįŠæČÜŅŗµĪČėŹÆČļŹŌŅŗ£¬ČÜŅŗ±äŗģ£¬ĘäŌŅņŹĒ ”£
£Ø2£©H2O2Ńõ»ÆFe2+µÄĄė×Ó·½³ĢŹ½ĪŖ ”£
£Ø3£©”°³żĢś”±Ź±£¬ČÜŅŗµÄpHÓ¦µ÷Õūµ½ £ØĻą¹Ų½šŹōĄė×ÓÉś³ÉĒāŃõ»ÆĪļ³ĮµķµÄpH¼°³ĮµķĶźČ«µÄpHČēĻĀ±ķ£¬½šŹōĄė×ÓæŖŹ¼³ĮµķŹ±µÄÅضČĪŖ1mol”¤L£1£©”£
| ½šŹōĄė×Ó | æŖŹ¼³ĮµķµÄpH | ³ĮµķĶźČ«µÄpH |
| Fe3+ | 1.1 | 3.2 |
| Zn2+ | 5.5 | 8.0 |
| Cu2+ | 5.2 | 6.7 |
| Fe2+ | 5.8 | 8.8 |
£Ø4£©”°³żĆĢ”±Ź±ČÜŅŗÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø5£©ŹŌ¼ĮXĪŖ ”£
£Ø6£©ÓÉZnSO4ČÜŅŗŠč¾¹ż£ŗ ”¢ ”¢¹żĀĖ¼°øÉŌļµĆZnSO4”¤7H2O”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijĪĀ¶ČĻĀ£¬Ļņ2 LŗćČŻĆܱÕČŻĘ÷ÖŠ³äČė1.0 mol A
ŗĶ1.0 mol B£¬·“Ó¦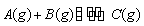 ¾¹żŅ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā”£·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄ²æ·ÖŹż¾Ż¼ūĻĀ±ķ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
¾¹żŅ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā”£·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄ²æ·ÖŹż¾Ż¼ūĻĀ±ķ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
| t£Æs | 0 | 5 | 15 | 25 | 35 |
| n(A)£Æmol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
A”¢·“Ó¦ŌŚĒ°5 sµÄĘ½¾łĖŁĀŹ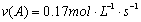
B”¢±£³ÖĘäĖūĢõ¼ž²»±ä£¬ÉżøßĪĀ¶Č£¬Ę½ŗāŹ± £¬Ōņ·“Ó¦µÄ
£¬Ōņ·“Ó¦µÄ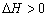
C”¢ĻąĶ¬ĪĀ¶ČĻĀ£¬ĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė2.0 mol C“ļµ½Ę½ŗāŹ±£¬CµÄ×Ŗ»ÆĀŹ“óÓŚ80£„
D”¢ĻąĶ¬ĪĀ¶ČĻĀ£¬ĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė0.20 mol A”¢0.20 mol BŗĶ1.0 mol C£¬·“Ó¦“ļµ½Ę½ŗāĒ°
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŵ±“¶ūĪļĄķѧ½±ŹŚÓč”°¹āĻĖÖ®øø”±Ó¢¹ś»ŖŅįæĘѧ¼ŅøßļæŅŌ¼°Į½Ī»ĆĄ¹śæĘѧ¼ŅĶžĄµĀ·²©ŅĮ¶ūŗĶĒĒÖĪ·Ź·ĆÜĖ¹”£¹āµ¼ĻĖĪ¬µÄÖ÷ŅŖ³É·ÖŹĒ¶žŃõ»Æ¹č£¬ĻĀĮŠ¹ŲÓŚ¶žŃõ»Æ¹čµÄĖµ·ØÕżČ·µÄŹĒ(””””)
A£®¶žŃõ»Æ¹čŹĒH2SiO3µÄĖįōū£¬Ņņ“ĖÄÜÓėĖ®·“Ó¦
B£®ÓƶžŃõ»Æ¹čÖĘČ”µ„ÖŹ¹čŹ±£¬µ±Éś³É2.24 L(±źæö)ĘųĢåŹ±£¬µĆµ½2.8 g¹č
C£®6 gµÄ¶žŃõ»Æ¹čÖŠŗ¬ÓŠ0.2 molµÄ¹²¼Ū¼ü
D£®¶žŃõ»Æ¹č²»ÄÜÓėĢ¼ĖįÄĘČÜŅŗ·“Ó¦£¬µ«ÄÜÓėĢ¼ĖįÄĘ¹ĢĢåŌŚøßĪĀŹ±·¢Éś·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijŠ£»ÆѧŹµŃéŠĖȤŠ”×éĪŖĮĖĢ½¾æŌŚŹµŃéŹŅÖʱøCl2µÄ¹ż³ĢÖŠ»įÓŠĖ®ÕōĘųŗĶHCl»Ó·¢³öĄ“£¬Ķ¬Ź±ŃéÖ¤ĀČĘųµÄijŠ©ŠŌÖŹ£¬¼×Ķ¬Ń§Éč¼ĘĮĖČēĶ¼ĖłŹ¾µÄŹµŃé×°ÖĆ(Ö§³ÅÓƵÄĢś¼ÜĢØŅŃŹ”ĀŌ)£¬°“ŅŖĒó»Ų“šĪŹĢā”£
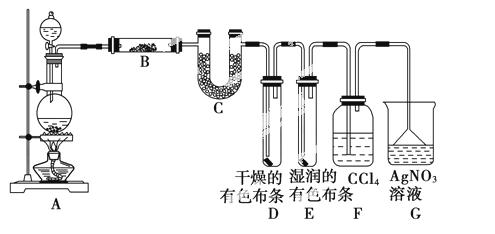
(1)ČōÓĆŗ¬ÓŠ0.2 mol HClµÄÅØŃĪĖįÓė×ćĮæµÄMnO2·“Ó¦£¬ÖʵƵÄCl2µÄĢå»ż(±ź×¼×“æöĻĀ)×ÜŹĒŠ”ÓŚ1.12 LµÄŌŅņŹĒ_______________________________________________________________________________”£
(2)¢Ł×°ÖĆBÖŠŹ¢·ÅµÄŹŌ¼ĮĆū³ĘĪŖ________£¬×÷ÓĆŹĒ_______________________________________”£
×°ÖĆCÖŠŹ¢·ÅµÄŹŌ¼ĮĆū³ĘĪŖ________£¬×÷ÓĆŹĒ_____________________________________________”£
¢Ś×°ÖĆDŗĶEÖŠ³öĻÖµÄĻÖĻó²»Ķ¬ĖµĆ÷µÄĪŹĢāŹĒ________________________________________ ”£
ӣ
¢Ū×°ÖĆFµÄ×÷ÓĆŹĒ_____________________________________”£
¢ÜŠ“³ö×°ÖĆGÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½__________________”£
(3)ŅŅĶ¬Ń§ČĻĪŖ¼×Ķ¬Ń§µÄŹµŃéӊȱĻŻ£¬²»ÄÜČ·±£×īÖÕĶØČėAgNO3ČÜŅŗÖŠµÄĘųĢåÖ»ÓŠŅ»ÖÖ”£ĪŖĮĖČ·±£ŹµŃé½įĀŪµÄæÉææŠŌ£¬Ö¤Ć÷×īÖÕĶØČėAgNO3ČÜŅŗµÄĘųĢåÖ»ÓŠŅ»ÖÖ£¬ŅŅĶ¬Ń§Ģį³öŌŚÄ³Į½øö×°ÖĆÖ®¼äŌŁ¼ÓŅ»øö×°ÖĆ”£ÄćČĻĪŖøĆ×°ÖĆÓ¦¼ÓŌŚ________Óė________Ö®¼ä(Ģī×°ÖĆ×ÖÄøŠņŗÅ)£¬×°ÖĆÖŠÓ¦·ÅČė________(ĢīŠ“ŹŌ¼Į»ņÓĆĘ·Ćū³Ę)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ³żŌÓ·½°ø“ķĪóµÄŹĒ
| Ń”Ļī | ±»Ģį“æµÄĪļÖŹ | ŌÓÖŹ | ³żŌÓŹŌ¼Į | ³żŌÓ·½·Ø |
| A | CO(g) | CO2(g) | NaOH ČÜŅŗ”¢ÅØ H2SO4 | Ļ“Ęų |
| B | NH4Cl(aq) | Fe3£«(aq) | NaOHČÜŅŗ | ¹żĀĖ |
| C | Cl2(g) | HCl(g) | ±„ŗĶŹ³ŃĪĖ®”¢ÅØH2SO4 | Ļ“Ęų |
| D | Na2CO3(s) | NaHCO3(s) | — | ×ĘÉÕ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””””)
A£®±½²»ÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶĖÉ«£¬Óė¼×ĶéŠŌÖŹĻąĖĘ£¬Ņņ“Ė±½ĪŖ±„ŗĶĢž
B£®±½µÄ½į¹¹¼ņŹ½ĪŖ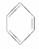 £¬ÓŠČżøöĖ«¼ü£¬æÉÓėäåĖ®·¢Éś¼Ó³É
£¬ÓŠČżøöĖ«¼ü£¬æÉÓėäåĖ®·¢Éś¼Ó³É
C£®±½µÄĮŚĪ»¶žŌŖČ”“ś²śĪļÖ»ÓŠŅ»ÖÖ
D£®±½µÄĮŚĪ»¶žŌŖČ”“ś²śĪļÓŠĮ½ÖÖ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com