
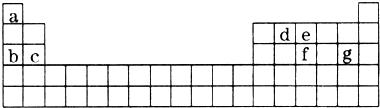
分析 由元素在周期表中位置,可知a为H、b为Na、c为Mg、d为C、e为N、f为P、g为Cl.
(1)同周期自左而右金属性减弱、同主族自上而下金属性增强;高氯酸的酸性最强;
(2)①一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键;
②所有原子都满足最外层为8电子结构,一定不含H,元素原子最外层电子+|化合物中该元素化合价|=8,化合物中该元素原子满足8电子结构;
(3)①处于金属与非金属交界处的元素具有一定金属性、非金属性,可以左半导体材料;
②Ga位于周期表的第ⅢA族其最高正价为+3价,As位于周期表的第VA族,负价为-3价,据此书写化学式;
(4)①由第三周期氢化物易燃性可知,元素非金属性越弱,氢化物越易燃;
②由题目信息可知,同主族元素与其它相同元素形成化合物自上而下毒性增强;
(5)①金属铍与铝的单质及其化合物性质相似,则Be与NaOH溶液反应生成Na2BeO2和氢气;
②氢氧化铍与氢氧化铝性质相似,能和氢氧化钠反应,而Mg(OH)2和氢氧化钠不反应.
解答 解:由元素在周期表中位置,可知a为H、b为Na、c为Mg、d为C、e为N、f为P、g为Cl.
(1)同周期自左而右金属性减弱、同主族自上而下金属性增强,故上述元素中Na的金属性最强;最高价含氧酸中HClO4的酸性最强,
故答案为:Na;HClO4;
(2)①元素的原子间反应最容易形成离子键的是b和g(NaCl),故答案为:B;
②所有原子都满足最外层为8电子结构,一定不含H,元素原子最外层电子+|化合物中该元素化合价|=8,化合物中该元素原子满足8电子结构,则所有原子都满足最外层为8电子结构的任意一种分子的分子式为CCl4、PCl3等,
故答案为:CCl4;PCl3;
(3)①在周期表里金属和非金属的交界处找到半导体材料,Si和Ge在金属和非金属的交界处可以作半导体,S是非金属性较强的元素,不能作半导体;
故答案为:C;
②Ga位于周期表的第ⅢA族其最高正价为+3价,As位于周期表的第VA族,负价为-3价,则二者形成的化合物为GaAs;
故答案为:GaAs;
(4)①由第三周期氢化物易燃性可知,元素非金属性越弱,氢化物越易燃,氢化物的易燃性:第二周期 CH4>NH3>H2O,
故答案为:CH4;
②由毒性:PH3>NH3、CS2>CO2、CC14>CF4可知同主族元素与其它相同元素形成化合物自上而下毒性增强,故毒性 H2S>H2O,
故答案为:>;
(5)①金属铍与铝的单质及其化合物性质相似,则Be与NaOH溶液反应生成Na2BeO2和氢气,离子反应为Be+2OH-=BeO22-+H2↑,
故答案为:Be+2OH-=BeO22-+H2↑;
②氢氧化铍与氢氧化铝性质相似,能和氢氧化钠反应,而Mg(OH)2和氢氧化钠不反应,则选NaOH溶液鉴别,故答案为:氢氧化钠溶液.
点评 本题考查元素周期表与元素周期律综合应用,是对学生综合能力的考查,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 2.52 g三聚氰胺含氮原子数目为0.12NA | |
| B. | 标准状况下1 mol的三聚氰胺的体积为22.4 L | |
| C. | 三聚氰胺含氮量约为10% | |
| D. | 三聚氰胺的摩尔质量为126 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (3)(5)(8) | B. | (5)(7)(8) | C. | (5)(8) | D. | (3)(5)(7)(8) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com