

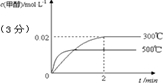
| ��c(H2) |
| ��t |
| 0.04mol/L |
| 2min |
| 0.04mol |
| 0.20mol |
| c(CHOH) |
| c(CO)?c2(H2) |
| 0.02mol/L |
| 0.08mol/L��0.25mol/L2 |
| c(CHOH) |
| c(CO)?c2(H2) |
| 0.02mol/L |
| 0.08mol/L��0.25mol/L2 |
| c(CHOH) |
| c(CO)?c2(H2) |
| 0.50 |
| 0.25��0.502 |
| c(CHOH) |
| c(CO)?c2(H2) |
| 0.02mol/L |
| 0.08mol/L��0.25mol/L2 |
 ��
��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����е�I2Ϊ��̬�����е�I2Ϊ��̬ |
| B���ڵķ�Ӧ���������Ȣٵķ�Ӧ���������� |
| C���ٵIJ���ȷ�Ӧ�ڵIJ������ȶ��Ը��� |
| D��1mol��̬������ʱ������17kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��H2��F2��Ӧ���Ȼ�ѧ����ʽΪ��H2��g��+F2��g��=2HF��g����H=-541kJ |
| B��44.8LHF����ֽ��22.4LH2��22.4LF2����541kJ������ |
| C��1molH2��1molF2��Ӧ����2molҺ̬HF�ų�������С��541kJ |
| D������ͬ�����£�1molH2��1molF2�������ܺʹ���2molHF��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������������ı��˷�Ӧ��;������Ӧ�ġ�HҲ��֮�ı� |
| B���ı�ѹǿ��ƽ�ⲻ�����ƶ�����Ӧ�ų����������� |
| C�������¶ȣ���Ӧ���ʼӿ죬��Ӧ�ų����������� |
| D������ԭ����н��У���Ӧ�ų����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
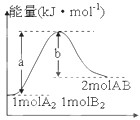
| A��ÿ����2����AB����bkJ���� |
| B���÷�Ӧ�ʱ�Ϊ��H=+��a-b��kJ/mol |
| C���÷�Ӧ�з�Ӧ�������������������������� |
| D������1molA-A����1molB-B�����ų�akJ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ȷ�Ӧ����Ҫ���ȾͿ��Է��� |
| B����ѧ��Ӧ���������������⣬�������������ı仯 |
| C����Ӧ����Ϊ���ȵķ�Ӧ�������ȷ�Ӧ |
| D����ѧ��Ӧ���Ȼ������ȣ�ȡ���ڷ�Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
| 1 |
| 2 |
| 2 |
| 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
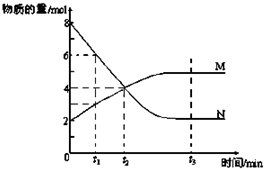
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com