
������ʵ������ó��Ľ�����ȷ���ǣ�
| ���������� | ���� | |
| A | ��AgCl����Һ�м���NaI��Һʱ���ֻ�ɫ������ | Ksp��AgCl��< Ksp��AgI�� |
| B | ��ij��Һ�еμ���ˮ���ټ���KSCN��Һ����Һ�ʺ�ɫ�� | ��Һ��һ������Fe2+ |
| C | ��NaBr��Һ�е���������ˮ�ͱ��������ã���Һ�ϲ�ʳȺ�ɫ�� | Br—��ԭ��ǿ��Cl— |
| D | ����ʢ��NH4Cl������Թܣ��Թܵײ�������ʧ���Թܿ��о������ᡣ | NH4Cl����������� |
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
֤������������Ԫ�صĴ��ڣ������м���������ȷ�IJ���˳����________(�����)��
�ټ�����������Һ���ڼ�������������Һ���ۼ��ȡ��ܼ�������ˮ���ݼ���ϡ��������Һ�����ԡ������������ƴ���Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����-ϩȲ���칹��Ӧ������Name Reactions����¼���÷�Ӧ�ɸ�Ч������Ԫ�������

��R��R����R����ʾ�⡢�������
�ϳ���Ԫ���л�������J��·�����£�
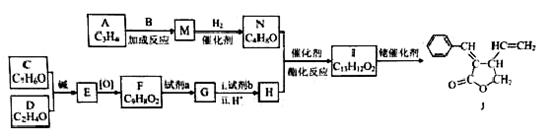
��֪��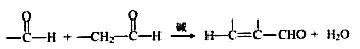
��1��A����Ȳ������ṹ��ʽ�� ��
��2��B��̼���⡢������Ԫ����ɣ���Է���������30��B�Ľṹ��ʽ��
��3��C��D������B��ͬ�Ĺ����ţ�C�Ƿ����廯���E�к��еĹ�������
��4��F���Լ�a��Ӧ����G�Ļ�ѧ����ʽ�� ���Լ�b�� ��
��5��M��N��Ϊ�����ʹ���M�Ľṹ��ʽ��
��6��NΪ˳ʽ�ṹ��д��N��H����I��˳ʽ�ṹ���Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵������ȷ����
A�� Na��H2O�ķ�Ӧ�������ķ��ȷ�Ӧ���÷�Ӧ���Է�����
B�� ����Na2SO4��Һ��Ũ�������ʹ��������Һ������������ԭ����ͬ
C�� FeCl3��MnO2���ɼӿ�H2O2�ֽ⣬ͬ�������¶��߶�H2O2�ֽ����ʵĸı���ͬ
D�� Mg(OH)2��������Һ�д���ƽ�⣺Mg(OH)2(s) Mg2+(aq)+2OH��(aq)���ù��������NH4Cl��Һ
Mg2+(aq)+2OH��(aq)���ù��������NH4Cl��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
FeCl3 ���о�ˮ���ã�����ʴ�豸�����ۺ��Ȼ�����һ�����͵���������������ˮ��FeCl3 ��Ч���Ҹ�ʴ��С����ش��������⣺
��1��FeCl3 ��ˮ��ԭ���� ��FeCl3 ��Һ��ʴ�����豸����H�������⣬��һ��Ҫԭ���ǣ������ӷ���ʽ��ʾ�� ��
��2��Ϊ��Լ�ɱ�����ҵ����NaClO3 ��������FeCl2 ��Һ�õ�FeCl3 ��
��������FeCl2 ��Һ��c(Fe2��)=2.0��10-2mol��L-1, c(Fe3��)=1.0��10-3mol��L-1, c(Cl��)=5.3��10-2mol��L-1,�����Һ��PHԼΪ ��
�����NaClO3 ����FeCl2 �����ӷ���ʽ��
| |
 ClO3-+
ClO3-+
|
 Fe2��+
Fe2��+ | |
 =
= | |
 Cl��+
Cl��+ | |
 Fe3��+
Fe3��+ | |
 .
. ��3��FeCl3 ����Һ�з�����ˮ�⣺
Fe3��+H2O  Fe(OH)2++H�� K1
Fe(OH)2++H�� K1
Fe(OH)2++H2O Fe(OH)2++H�� K2
Fe(OH)2++H�� K2
Fe(OH)++H2O Fe(OH)3+H�� K3
Fe(OH)3+H�� K3
����ˮ�ⷴӦ��ƽ�ⳣ��K1��K2��K3�ɴ�С��˳���� ��
ͨ����������������ˮ�����ۺϣ����ɾۺ������������ӷ���ʽΪ��
xFe3++yH2O Fex(OH)y(3x-y)++yH+
Fex(OH)y(3x-y)++yH+
 ��ʹƽ�������ƶ��ɲ��õķ����ǣ�����ţ� ��
��ʹƽ�������ƶ��ɲ��õķ����ǣ�����ţ� ��
a.���� b.��ˮϡ�� c.����NH4Cl d.����NaHCO3
�����£�ʹ�Ȼ�����Һת��Ϊ��Ũ�Ⱦۺ��Ȼ����Ĺؼ������� ��
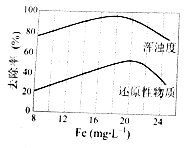
��4�����ij��ˮ���������Ȼ���������ˮ�Ľ������ͼ��ʾ����ͼ�����ݵó�ÿ����ˮ��Ͷ�žۺ��Ȼ���[��Fe(mg��L-1)��ʾ]����ѷ�ΧԼΪ mg��L-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʯ����Ҫ�ɷ�BaCO3����Ca2+��Mg2+��Fe3+�����ʣ���ʵ�������ö���ʯ�Ʊ�BaCl2·2H2O����������:
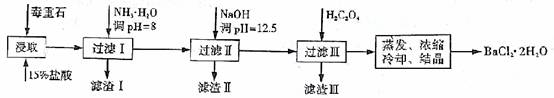
��1������ʯ�������ȡǰ������ĥ��Ŀ���� ��ʵ������37%����������15%�����ᣬ����Ͳ���ʹ�����������е� ��
a���ձ� b������ƿ c�������� d���ζ���
��2��
| Ca2+ | Mg2+ | Fe3+ | |
| ��ʼ����ʱ��pH | 11.9 | 9.1 | 1.9 |
| ��ȫ����ʱ��pH | 13.9 | 11.1 | 3.2 |
����NH3·H2O����pH=8�ɳ�ȥ �������ӷ��ţ����������к� ���ѧʽ��������H2C2O4ʱӦ���������ԭ���� ��
��֪��Ksp��BaC2O4��=1.6��10-7��Ksp��CaC2O4��=2.3��10-9
��3�����ü�����ζ����ɲⶨBa2+�ĺ�����ʵ����������С�
��֪��2CrO42—+2H+=Cr2O72—+H20 Ba2++CrO42—=BaCrO4��
����� ��ȡxmlһ��Ũ�ȵ�Na2CrO4��Һ����ƿ�У��������ָʾ������b mol·L��1�����Һ�ζ����յ㣬��õμ��������ΪV0mL��
�������ȡy mLBaCl2��Һ����ƿ�У�����x mL�벽��� ��ͬŨ�ȵ�Na2CrO4��Һ����Ba2+��ȫ�������ټ������ָʾ������b mol·L��1�����Һ�ζ����յ㣬��õμ���������ΪV1mL��
�μ������ҺʱӦ����ʽ�ζ��ܣ���0���̶�λ�ڵζ��ܵ� ����Ϸ������·�������BaCl2��Һ��Ũ��Ϊ mol·L��1����������еμ�����ʱ����������Һ������Ba2+Ũ�Ȳ���ֵ�� ���ƫ��ƫС������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ZEBRA�����صĽṹ��ͼ��ʾ���缫���϶��Ni/NiCl2�ͽ�����֮���������ӵ����������մɹ���������й��ڸõ�ص������������(����)
A����ط�Ӧ����NaCl����
B����ص��ܷ�Ӧ�ǽ����ƻ�ԭ����������
C��������ӦΪ��NiCl2��2e��===Ni��2Cl��
D��������ͨ�������ӵ��������缫���ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��2L�����ܱ�������Ͷ������M(s)��һ������R(g)��������ӦΪ
M(s)��R(g) X(g)��Y(g)
X(g)��Y(g) 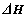 ������ʵ���������±���ʾ��
������ʵ���������±���ʾ��
| ʵ�� | �¶�/�� | ��ʼʱR�����ʵ���/mol | ƽ��ʱ���������ʵ���/mol |
| �� | 300 | 2.00 | 2.80 |
| �� | 400 | 2.00 | 3.00 |
| �� | 400 | 4.00 | a |
�����ƶ���ȷ����
A��������Ӧ�У�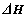 ��0
��0
B��ʵ����У��÷�Ӧ��ƽ�ⳣ��K��0.5
C��ʵ��پ�4 min�ﵽƽ�⣬0��4 min�ڦ�(X)��0.2mol•L1•min1
D��ʵ�����a��6.00
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ʵ���ܴﵽԤ��Ŀ�ĵ���(����)
| ѡ�� | ʵ������ | ʵ��Ŀ�� |
| A | �ζ�ʵ���У��ô���Һ��ϴ��ƿ2��3�� | �������ʵ����� |
| B | ����ˮ�еμ�AgNO3��ϡHNO3��Һ��������ɫ���� | ��֤��ˮ�к���Cl�� |
| C | ��ʢ�з�ˮ���ձ��еμӱ����Ȼ�����Һ����ʱ����� | �Ʊ������������� |
| D | ��2 mL 1 mol��L��1 NaOH��Һ���ȼ���3��1 mol��L��1 MgCl2��Һ���ټ���3��1 mol��L��1 FeCl3��Һ | ֤��Mg(OH)2��������ת��ΪFe(OH)3���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com