
【题目】取50.0mL的碳酸钠和硫酸钠的混合溶液,加入过量氯化钡溶液后得到14.51g白色沉淀,用过量稀硝酸处理后沉淀量减少到4.66g,并有气体放出。试计算:
(1)原混合液中碳酸钠和硫酸钠的物质的量浓度。
(2)产生气体的质量
【答案】
(1)c(Na2CO3)=1.0mol/Lc(Na2SO4)=0.4mol/L,
(2)2.2g
【解析】
试题分析:混合液加入过量BaCl2溶液后,发生Na2CO3+BaCl2=BaCO3↓+2NaCl,Na2SO4+BaCl2=BaSO4↓+2NaCl,故14.51克白色沉淀是BaCO3和BaSO4混合物,加入过量的稀HNO3,发生反应:BaCO3+2HNO3=Ba(NO3)2+CO2↑+H2O,剩余沉淀4.66g为BaSO4。
(1)n(Na2SO4)=n(BaSO4)=![]() =0.02mol,所以c(Na2SO4)=
=0.02mol,所以c(Na2SO4)=![]() =0.4mol/L,
=0.4mol/L,
m(BaCO3)=14.51g-4.66g=9.85g,n(Na2CO3)=n(BaCO3)=![]() =0.05mol,
=0.05mol,
所以c(Na2CO3)=![]() =1mol/L,答:原混和溶液中Na2CO3的物质的量浓度分别为1mol/L,Na2SO4的物质的量浓度为0.4mol/L;
=1mol/L,答:原混和溶液中Na2CO3的物质的量浓度分别为1mol/L,Na2SO4的物质的量浓度为0.4mol/L;
(2)n(CO2)=n(BaCO3)=0.05mol,故m(CO2)=0.05mol×44g/mol=2.2g,答:生成气体的质量为2.2g。


科目:高中化学 来源: 题型:
【题目】某硫原子的质量是ag,一个12C原子的质量是bg,若NA只表示阿伏加德罗常教的数值,则下列说法中正确的是()
①该硫原子的相对原子质量为12a/b
②m g该硫原子的物质的量为m/aNA mol
③该硫原子的摩尔质量是aNAg/mol
④ ag该硫原子所含的电子数为16
⑤cg 该硫原子所含质子数为4bcNA/3a
A.①②③④⑤ B.①②③④ C.①②④⑤ D.①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】框图中甲、乙为单质,其余均为化合物,B为常见液态化合物,A为淡黄色固体,F、G所含元素相同且均为氯化物,G遇KSCN溶液显红色。
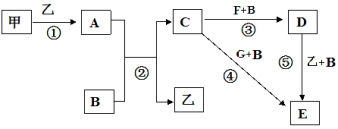
请问答下列问题:
(1)反应①-⑤中,既属于氧化还原反应又属于化合反应的是______________(填序号)。
(2)反应⑤的化学方程式为____________________________。
(3)甲与B反应的离子方程式 ______________________________。
(4)在实验室将C溶液滴入F溶液中,观察到的现象是_____________。
(5)在F溶液中加入等物质的量的A,发生反应的总的离子方程式为:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2SO2(g)+O2(g)![]() 2SO3(g)ΔH=-197k/mol。在相同的温度下,向体积相同的三个密闭容器中分别充入气体:(甲)2molSO2和1molO2;(乙)1molSO2和0.5molO2;(丙)2molSO3。反应达平衡时,下列关系一定正确的是
2SO3(g)ΔH=-197k/mol。在相同的温度下,向体积相同的三个密闭容器中分别充入气体:(甲)2molSO2和1molO2;(乙)1molSO2和0.5molO2;(丙)2molSO3。反应达平衡时,下列关系一定正确的是
A.容器内压强P:P甲=P丙> 2P乙
B.SO3的质量m:m甲=m丙> 2m乙
C.c(SO2)与c(O2)之比k:k甲=k丙> k乙
D.反应放出或吸收热量的数值Q:Q甲=Q丙> 2Q乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,腐蚀严重的青铜器表面大都存在CuCl。关于CuCl在青铜器腐蚀过程中的催化作用,下列叙述正确的是________。
A. 降低了反应的活化能 B. 增大了反应的速率
C. 降低了反应的焓变 D. 增大了反应的平衡常数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用0.2mol/L的Na2SO3溶液60mL,恰好将4×10﹣3mol XO4﹣还原,则元素X在还原产物中的化合价是( )
A.+4
B.+3
C.+2
D.+1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电池的说法不正确的是( )
A. 太阳能电池的主要材料是高纯度的二氧化硅
B. 铜锌原电池工作时,电子沿外电路从锌电极流向铜电极
C. 氢氧燃料电池工作时,氢气在负极被氧化
D. 原电池中一定发生了氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com