
已知HCO3―+AlO2― +H2O=CO32― +Al(OH)3↓;将足量的KHCO3溶液不断滴入含等物质的量的KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与滴入的KHCO3溶液体积的关系可表示为
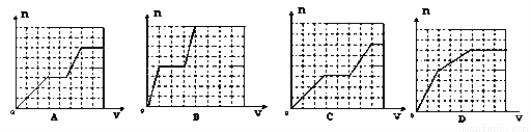
B
【解析】
试题分析:HCO3-先与OH-反应,再与AlO2-反应,而HCO3-与OH-反应生成CO32-后,Ba2+与CO32-生成沉淀,HCO3-+OH-+Ba2+═BaCO3↓+H2O①,消耗1molHCO3-、1molOH-、1molBa2+,生成1molBaCO3沉淀,此阶段化学方程式为KHCO3+Ba(OH)2═BaCO3↓+H2O+KOH;HCO3-+OH-═CO32-+H2O②,消耗2mol HCO3-、2molOH- (OH-消耗完),没有沉淀生成.此阶段化学方程式为KHCO3+KOH=K2CO3+H2O(此时KOH有2mol,原溶液中有1mol,反应①产生1mol);HCO3-+AlO2-+H2O═CO32-+Al(OH)3↓③,消耗1molHCO3-、1mol AlO2-(AlO2-消耗完),生成1molAl(OH)3沉淀.此阶段化学方程式为KHCO3+KAlO2+H2O═Al(OH)3↓+K2CO3.三阶段消耗KHCO3的物质的量为1:2:1,也即KHCO3溶液体积比为1:2:1;一、三阶段对应的生成沉淀的物质的量为1:1,第二阶段不生成沉淀,所以图象B符合,答案选B。
考点:考查离子方程式的计算


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2013-2014宁夏银川市高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
莽草酸的结构简式如图,下列关于莽草酸的说法不正确的是
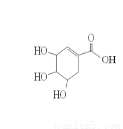
A.相同条件下等物质的量的莽草酸和正戊醛(C5H10O)完全燃烧时的耗氧量相同
B.分子中含有两种含氧官能团,可发生取代反应
C.1mol莽草酸既可与2mol氢气发生加成反应,也可与4molNaOH发生中和反应
D.可用溴水鉴别莽草酸、乙醇、四氯化碳和苯
查看答案和解析>>
科目:高中化学 来源:2013-2014宁夏高一下学期期中考试化学试卷(解析版) 题型:选择题
已知下列元素的原子半径为
原子 |
|
|
|
|
半径 | 0.75 | 1.02 | 0.74 | 1.17 |
根据以上数据,磷原子的半径可能是( )
A.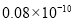 m B.
m B.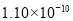 m C.
m C.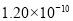 m D.
m D.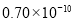 m
m
查看答案和解析>>
科目:高中化学 来源:2013-2014学年陕西省五校高三第三联考理综化学试卷(解析版) 题型:填空题
开发新型储氢材料是氢能利用的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Ti3+的未成对电子数有______个。
②LiBH4由Li+和BH4-构成,BH4-的等电子体是 (写一种)。LiBH4中不存在的作用力有___(填标号)。
A.离子键 B.共价键 C.金属键 D.配位键
③Li、B、H元素的电负性由大到小排列顺序为_ _____。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+______H-(填“>”、“=”或“<”)。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
I1/KJ·mol-1 | I2/KJ·mol-1 | I3/KJ·mol-1 | I4/KJ·mol-1 | I5/KJ·mol-1 |
738 | 1451 | 7733 | 10540 | 13630 |
M是______(填元素符号)。
(3)某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有____种。

(4)若已知元素电负性氟大于氧,试解释沸点H2O高于HF 。
分子X可以通过氢键形成“笼状结构”而成为潜在的储氢材料。X—定不是______(填标号)。
A.H2O B.CH4 C.HF D.CO(NH2)2
(5)纳米材料的表面粒子数占总粒子数的比例极大,这是它具有许多特殊性质的原因。假设某氯化钠纳米颗粒的大小和形状恰好与氯化钠晶胞的大小和形状相同。则这种纳米颗粒的表面粒子数占总粒子数的百分数为 。

A.87.5% B.92.9% C.96.3% D.100%
查看答案和解析>>
科目:高中化学 来源:2013-2014学年陕西省五校高三第三联考理综化学试卷(解析版) 题型:选择题
火法炼铜首先要焙烧黄铜矿,反应为:2CuFeS2+O2→Cu2S+2FeS+SO2 则下列说法正确的是
A.CuFeS2仅作还原剂,硫元素被氧化
B.每生成1mol Cu2S,有4 mol硫被氧化
C.SO2只是氧化产物,FeS只是还原产物
D.每转移1.2 mol电子,有0.2 mol硫被氧化
查看答案和解析>>
科目:高中化学 来源:2013-2014学年辽宁省东北三省高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
氯化铁和高铁酸钾都是常见的水处理剂。下图为制备氯化铁及进一步氧化制备高铁酸钾的工艺流程。
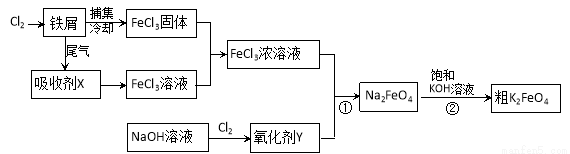
请回答下列问题:
(1)氯化铁有多种用途,请用离子方程式表示下列用途的原理。
①氯化铁做净水剂______________________;
②用FeCl3溶液(32%~35%)腐蚀铜印刷线路板____________________________。
(2)吸收剂X的化学式为 ;氧化剂Y的化学式为________________。
(3)碱性条件下反应①的离子方程式为____________________________________。
(4)过程②将混合溶液搅拌半小时,静置,抽滤获得粗产品。该反应的化学方程式为
2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析反应发生的原因_________。
(5)K2FeO4 在水溶液中易发生反应:4FeO42?+10H2O 4Fe(OH)3+8OH?+3O2↑。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 (填序号)。
4Fe(OH)3+8OH?+3O2↑。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 (填序号)。
A.H2O B.稀KOH溶液、异丙醇 C.NH4Cl溶液、异丙醇 D.Fe(NO3)3溶液、异丙醇
(6)可用滴定分析法测定粗K2FeO4的纯度,有关反应离子方程式为:
①FeO42?+CrO2? +2H2O CrO42?+Fe(OH)3↓+OH?
CrO42?+Fe(OH)3↓+OH?
②2CrO42?+2H+ Cr2O72?+H2O
Cr2O72?+H2O
③Cr2O72 ?+6Fe2++14H+ 2Cr3++6Fe3++7H2O
2Cr3++6Fe3++7H2O
现称取1.980 g粗高铁酸钾样品溶于适量氢氧化钾溶液中,加入稍过量的KCrO2,充分反应后过滤,滤液定容于250 mL容量瓶中。每次取25.00 mL加入稀硫酸酸化,用0.1000 mol/L的(NH4)2Fe(SO4)2标准溶液滴定,三次滴定消耗标准溶液的平均体积为18.93 mL。则上述样品中高铁酸钾的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年甘肃省玉门市高三第三次摸底考试化学试卷(解析版) 题型:选择题
若溶液中由水电离产生的c(OH-)=1×10-13mol/L,满足此条件的溶液中一定可以大量共存的离子组是 ( )
A.Al3+、Na+、NO3-、Cl- B.K+、Na+、Cl-、SO42-
C.K+、Na+、Cl-、CO32- D.K+、I-、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖南省益阳市高三下学期模拟考试理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
①常温常压下,18g14CH4所含中子数目为8 NA
②1L0.1mol·L-1的氨水中有NA个NH4+
③1mol Na2O2中含有NA个阴离子
④1L1mol·L-1NaClO 溶液中含有ClO-的数目为NA
⑤78g 苯含有C=C双键的数目为3NA
⑥0.1molN2和0.3molH2在某密闭容器中充分反应,转移电子的数目为0.6NA
⑦60gSiO2晶体中含有硅氧键的数目为4NA
A.①③⑦ B.②③⑥ C.②④⑥ D.①④⑤⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com