
| A. | 将58.5 g NaCl溶解于1 L 水中 | |
| B. | 将22.4 L氨气溶于水配成1 L溶液 | |
| C. | 将1 L 10 mol•L-1的浓盐酸与9 L水混合 | |
| D. | 将10 g NaOH溶解在水中配成250 mL溶液 |
分析 A、1L水中溶解了58.5g NaCl,溶液体积大于1L;
B、气体压强温度不知不能计算气体物质的量;
C.溶液体积不具有加合性;
D、质量换算物质的量,依据浓度概念计算得到.
解答 解:A、1L水中溶解了58.5g NaCl,溶液体积大于1L,该溶液的物质的量浓度小于1mol•L-1,故A错误;
B、气体压强温度不知不能计算气体物质的量,故B错误;
C.溶液体积不具有加合性,混合后溶液的体积不是10L,故C错误;
D、10gNaOH物质的量为0.25mol,溶解后配制为250ml的溶液,其浓度为1 mol•L-1,故D正确;
故选D.
点评 本题考查了溶液浓度的计算应用,主要是溶液混合后体积变化的判断,浓度概念的理解分析,题目难度中等.


科目:高中化学 来源: 题型:解答题
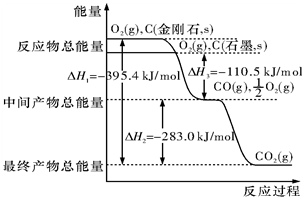 金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示.
金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 参加离子反应的一定都是电解质 | |
| B. | 任何一种离子的浓度在离子反应中一定变小 | |
| C. | 自由离子之间的反应不能在固态中进行 | |
| D. | 没有沉淀、气体、水生成的反应就不是离子反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
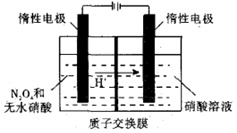 N2O5是绿色硝化试剂,溶于水可得硝酸.图是以N2O4为原料电解制备N2O5的装置示意图写出阳极区生成N2O5的电极反应式是N2O4-2e-+2HNO3=2N2O5+2H+.
N2O5是绿色硝化试剂,溶于水可得硝酸.图是以N2O4为原料电解制备N2O5的装置示意图写出阳极区生成N2O5的电极反应式是N2O4-2e-+2HNO3=2N2O5+2H+.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若a=b+c时,B的物质的量分数变大 | B. | 若a=b+c时,B的物质的量分数变小 | ||
| C. | 若a>b+c时,A的转化率不变 | D. | 若a<b+c时,A的转化率变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2+CaO$\frac{\underline{\;高温\;}}{\;}$CaSiO3 | |
| B. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C | |
| C. | N2+3H2$?_{△}^{催化剂}$2NH3 | |
| D. | C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径(×10-10m) | 0.37 | 1.86 | 1.43 | 0.99 | 0.75 | 0.74 | |
| 主要化合价 | 最高正价 | +1 | +1 | +3 | +7 | +5 | \ |
| 最低负价 | -1 | \ | \ | -1 | -3 | -2 | |
| A. | 元素X、Z、R的离子均能影响水的电离平衡 | |
| B. | Y、Z、M、R四种元素的最高价氧化物的水化物两两之间会发生反应 | |
| C. | 化合物XM、YM都是电解质,熔融状态下都能导电 | |
| D. | 离子半径大小:M>Y>Z>R |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com