
【题目】某固体混合物可能由Al、MgCl2、AlCl3、FcCl2中的一种或几种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):

回答下列问题:
(1)混合物中是否存在FeCl2: ___________(填“是”或“否”)。
(2)写出反应④的离子方程式:_____________
(3)请判断混合物中是否含有AlCl3(如不含,简述依据;如含有,写出所含AlCl3的质量)__________。
【答案】 否 Al(OH)3+3H+=Al3++2H2O 含13.2g
【解析】本题考查无机推断,混合物中加入过量NaOH溶液,产生气体,说明混合物中含有Al,且Al的物质的量为2×6.72/(3×22.4)mol=0.2mol,质量为5.4g,Mg2+与OH-反应生成Mg(OH)2↓,Fe2+与OH-生成Fe(OH)2↓,久置后,白色沉淀迅速转变为红褐色沉淀,但根据转化关系,无明显变化,说明混合物中没有FeCl2,沉淀为Mg(OH)2,根据元素守恒,MgCl2的质量为5.8×95/58g=9.5g,混合物的质量为28.1g,因此推出含有AlCl3,其质量为(28.1-5.4-9.5)g=13.2g,(1)根据上述分析,混合物中不含FeCl2;(2)无色溶液中加入稀盐酸,产生Al(OH)3,继续加入稀盐酸,发生Al(OH)3+3H+=Al3++3H2O;(3)根据上述分析,混合物中含有AlCl3,其质量为13.2g。


科目:高中化学 来源: 题型:
【题目】草酸是植物(特别是草本植物)常具有的成分,具有广泛的用途。草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数K1=5.4×10-2,K2=5.4×10-5。回答下列问题:
(1)拟用下列装置分解草酸制备少量纯净的CO,其合理的连接顺序为___________(填字母序号)。


![]()


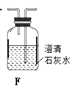
(2)相同温度条件下,分别用3支试管按下列要求完成实验:
试管 | A | B | C |
加入试剂 | 4mL 0.01mol/L KMnO4 1ml 0.1moL/L H2SO4 2mL 0.1mol/L H2C2O4 | 4mL 0.02mol/L KMnO4 1ml 0.1moL/L H2SO4 2mL 0.1mol/L H2C2O4 | 4mL 0.03mol/L KMnO4 1ml 0.1moL/L H2SO4 2mL 0.1mol/L H2C2O4 |
褪色时间 | 28秒 | 30秒 | 不褪色 |
写出试管B的离子方程式_____________________________________;上述实验能否说明“相同条件下,反应物浓度越大,反应速率越快”?____________(选填“能”或“不能”);简述你的理由:__________________________________。
(3)设计实验证明草酸为弱酸的方案及其现象均正确的有_____________(填序号)。
A.室温下,取0.010mol/L的H2C2O4溶液,测其pH=2;
B.室温下,取0.010mol/L的NaHC2O4溶液,测其pH >7;
C.室温下,取pH=a(a<3)的H2C2O4溶液稀释100倍后,测其pH< a+2;
D.标况下,取0.10mol/L的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL;
(4)为测定某H2C2O4溶液的浓度,取20.00mL H2C2O4溶液于锥形瓶中,滴入2-3滴指示剂,用0.1000mol/L的NaOH溶液进行滴定,并进行3次平行实验,所用NaOH溶液体积分别为19.98mL、20.02mL和22.00mL。
①所用指示剂为_______________;滴定终点时的现象为_________________________;
②H2C2O4溶液物质的量浓度为_______________;
③下列操作会引起测定结果偏高的是__________(填序号)。
A. 滴定管在盛装NaOH溶液前未润洗
B. 滴定过程中,锥形瓶震荡的太剧烈,以致部分液体溅出
C. 滴定前读数正确,滴定终点时俯视读数
D. 滴定前读数正确,滴定终点时仰视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下,溶液中能发生如下反应:①2R-+Z2===R2+2Z- ②16H++10Z-+2XO![]() ===2X2++5Z2+8H2O ③2M2++R2===2M3++2R-。由此判断,下列说法中正确的是( )
===2X2++5Z2+8H2O ③2M2++R2===2M3++2R-。由此判断,下列说法中正确的是( )
A. Z2+2M2+===2M3++2Z-不可以进行
B. Z元素在①②反应中都发生还原反应
C. X2+是还原剂XO4—的还原产物
D. 各粒子氧化性由强到弱的顺序是XO![]() >Z2>R2>M3+
>Z2>R2>M3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用离子方程式H++OH-→H2O表示的反应是( )
A. 稀硫酸和氢氧化钾 B. 稀硫酸和氢氧化钡溶液
C. 氢硫酸和氢氧化钠溶液 D. 稀硝酸和氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题目信息完成下列方程式。
(1)已知硫酸铅(PbSO4)不溶于盐酸也不溶于硝酸,但可溶于醋酸铵(CH3COONH4)溶液中形成无色溶液,其化学方程式为PbSO4 + 2CH3COONH4 = (CH3COO)2Pb + (NH4)2SO4。当在(CH3COO)2Pb溶液中通入H2S气体时,有黑色PbS沉淀生成,则此反应的离子方程式为__________________.
(2)钛(Ti)因为具有神奇的性能越来越引起人们的关注。地壳中含钛铁矿石之一是金红石(TiO2),目前大规模生产的方法是:
第一步:金红石、炭粉混合,在高温条件下,通入Cl2制得TiCl4和一种可燃气体,该反应的化学方程式为:____________________________________________;
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。写出此反应的化学方程式:____________________________________________。
(3)用100mL 0.1mol/L的NaOH溶液吸收224mLCO2气体(标准状况),恰好完全吸收。再将所得溶液加入100mL 0.1mol/L氢氧化钙溶液中。请写出所得溶液与氢氧化钙溶液反应的离子方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M 转化为N 分两步完成:①M(g)+Q(s) ![]() R(s) ΔH1>0; ②M(g)+R(s)
R(s) ΔH1>0; ②M(g)+R(s) ![]() N(g)+Q(s) ΔH2<0。
N(g)+Q(s) ΔH2<0。
转化过程中的能量变化如图所示,下列说法正确的是

A. 反应②的逆反应的活化能为 E4 kJ·mol-1
B. 反应①的正反应的活化能一定大于 ΔH1
C. R 是该反应的催化剂
D. 2M(g) ![]() N(g)的 ΔH=(E5-E1) kJ·mol-1
N(g)的 ΔH=(E5-E1) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属能导电的原因是( )
A.金属晶体中金属阳离子与自由电子间的相互作用较弱
B.金属晶体中的自由电子在外加电场作用下发生定向移动
C.金属晶体中的金属阳离子在外加电场作用下可发生定向移动
D.金属晶体在外加电场作用下可失去电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验过程中产生的现象与如图所示座标图形相符合的是( )

A. 稀盐酸滴加到一定量NaHCO3,溶液中(横坐标是稀盐酸的体积,纵坐标为气体体积)
B. NaOH溶液滴入Ba(HCO3)2溶液中(横坐标是NaOH溶液的体积,纵坐标为沉淀质量)
C. 稀盐酸滴加到AgNO3溶液中(横坐标是稀盐酸的体积,纵坐标为溶液的导电能力)
D. 稀硫酸滴加到Ba(OH)2溶液中(横坐标是稀硫酸的体积,纵坐标为溶液的导电能力)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com