
| 编号 | 操作 | 现象 |
| Ⅰ | 先向2mL0.1mol•L-1FeCl2溶液中滴加KSCN溶液,再滴加新制氯水 | 滴加KSCN后溶液无明显变化, 加入氯水后溶液变成血红色. |
| Ⅱ | 先向2mL0.1mol•L-1FeCl3溶液中滴加KSCN溶液,再滴加0.1mol•L-1KI溶液 | 滴加KSCN溶液后,溶液变成血红色;滴加0.1mol•L-1KI溶液后,血红色无明显变化 |
| 编号 | 操作 | 现象 |
| Ⅲ | 向2mL0.1mol•L-1KI溶液中滴加1mL 0.1mol•L-1FeCl3溶液,再滴加KSCN溶液 | 滴加FeCl3溶液后,溶液变成黄色;滴加KSCN溶液后,溶液变成血红色 |
| 编号 | 操作 | 预期现象及结论 |
| Ⅳ | 向2mL0.1mol•L-1KI溶液中滴加1mL 0.1mol•L-1 FeCl3,溶液变黄色,取该溶液于两支试管中, 试管①中滴加滴加淀粉溶液(或CCl4), 试管②中滴加滴加铁氰化钾溶液. | 预期现象①溶液变蓝 (或溶液分层,下层溶液为紫红色),②出现特征蓝色沉淀. 结论Fe3+能与I-发生氧化还原反应,生成I2和Fe2+. |
分析 (1)亚铁离子和硫氰化钾溶液不反应,但亚铁离子有还原性,能被氯气氧化生成铁离子,铁离子和硫氰根离子反应生成血红色的络合物,导致溶液呈血红色;
(2)碘水溶液呈黄色,生成了碘单质,说明发生了氧化还原反应;
(3)如果碘离子和铁离子反应生成亚铁离子和碘单质,根据亚铁离子的特征反应或碘单质的特征反应进行实验,碘遇淀粉溶液变蓝色、碘溶于四氯化碳后溶液呈紫色,亚铁离子和铁氰化钾溶液反应生成蓝色沉淀;
(4)碘离子和铁离子发生氧化还原反应且参加反应的Fe3+与I-的物质的量相同,再结合得失电子数相等确定反应方程式.
解答 解:(1)①亚铁离子和硫氰化钾溶液不反应,所以向氯化亚铁溶液中滴加硫氰化钾溶液后,溶液不呈红色,再滴加氯水后,氯气把亚铁离子氧化呈铁离子,离子反应为:2Fe2++Cl2═2Fe3++2Cl-,铁离子和硫氰化钾溶液反应生成络合物,导致溶液呈血红色,离子反应为:Fe3++3SCN-=Fe(SCN)3,所以实验I的现象为滴加KSCN后溶液无明显变化,加入氯水后溶液变成红色,
故答案为:
| 编号 | 操作 | 现象 |
| Ⅰ | 滴加KSCN后溶液无明显变化 加入氯水后溶液变成血红色 | |
| Ⅱ |
| 编号 | 操作 | 预期现象及结论 |
| Ⅳ | 再滴加淀粉溶液(或CCl4) 滴加铁氰化钾溶液 | 预期现象:溶液变蓝 (或溶液分层,下层溶液为紫红色) 出现特征蓝色沉淀 结论:Fe3+能与I-发生氧化还原反应,生成I2和Fe2+ |
点评 本题考查了亚铁离子和铁离子之间的相互转化,题目难度中等,铁离子和亚铁离子的检验是高考的热点,根据铁离子和亚铁离子的特征反应来检验,注意掌握实验方案设计与评价的原则,试题培养了学生的分析能力及化学实验能力.


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:计算题
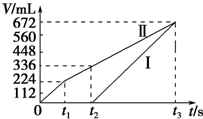 常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图中Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:(要求写出计算步骤)
常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图中Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:(要求写出计算步骤)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图,将一根较纯的铁棒垂直没入水中,由于深水处溶氧量较少,一段时间后发现AB段产生较多铁锈,BC段腐蚀严重.下列关于此现象的说法错误的是( )
如图,将一根较纯的铁棒垂直没入水中,由于深水处溶氧量较少,一段时间后发现AB段产生较多铁锈,BC段腐蚀严重.下列关于此现象的说法错误的是( )| A. | 该腐蚀过程属于电化腐蚀 | |
| B. | 铁棒AB段电极反应为O2+2H2O+4e→4OH- | |
| C. | 铁棒AB段是负极,BC段是正极 | |
| D. | 产生此现象的根本原因是铁棒所处化学环境的不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 .
. .
.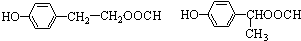 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在浓海水中存在反应 Br2+H2O?HBr+HBrO | |
| B. | 纯碱溶液显碱性的原因是 CO32-+2H2O?H2CO3+OH- | |
| C. | 海水中提取溴还可用到的反应 Cl2+2Br-═2Cl-+Br2 | |
| D. | 纯碱吸收溴的主要反应是3Br2+3Na2CO3═5NaBr+NaBrO3+3CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分类方法、统计方法、定量研究、实验方法和模型化方法等是化学研究的常用方法 | |
| B. | 电解熔融氧化铝、粗硅的制取、生物炼铜、煤焦油中提取苯等过程都涉及化学变化 | |
| C. | 从2016年1月1号开始浙江省汽油标准由“国Ⅳ”提高到“国V”,但这并不意味着汽车不再排放氮氧化物 | |
| D. | 纳米技术、分子设计技术的发展,将使分子晶体管、分子芯片、分子导线、分子计算机等化学器件得到广泛的应用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
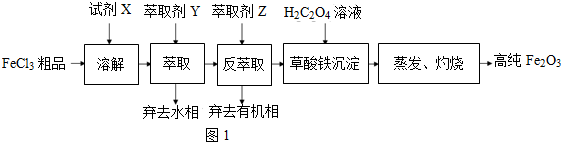
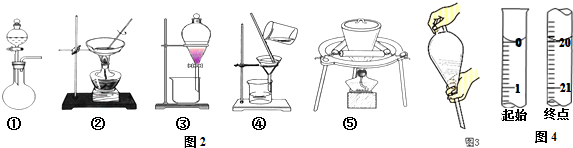
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将浓氨水加到盛有AgCl固体的试管中 | AgCl固体完全溶解 | 所得溶液中c(Ag+)•c(Cl-) ≤Ksp(AgCl) |
| B | 向FeI2溶液中通入少量的氯气,再向反应后的溶液中滴加KSCN溶液 | 溶液变为红色 | Cl2能将Fe2+氧化成Fe3+ |
| C | 向固体纯碱中滴加足量浓盐酸,将产生的气体通入苯酚钠溶液 | 溶液变浑浊 | 酸性:盐酸>碳酸>苯酚 |
| D | 向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均发生变性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
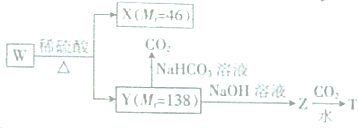
 +CO2+H2O→
+CO2+H2O→ +NaHCO3.
+NaHCO3.
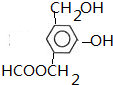 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com