
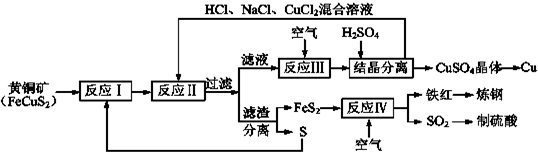
���� �����з�Ӧ��Ļ�ѧ������ΪCuFeS2+S�TFeS2+CuS����ͭ����S�ڸ��������գ�ʹ��ת��ΪFeS2��CuS������HCl��NaCl��CuCl2�����Һ ������ӦCu2++CuS+4Cl-=2[CuCl2]-+S�������˵õ���Һ��ͨ�����������Ӧ4CuCl2-+O2+4H+=4Cu2++8Cl-+2H2O��һ���¶��£��ڷ�Ӧ�����õ���Һ�м���ϡ���ᣬ������������ͭ���壬�ᾧ����õ�����ͭ���壬��������ԭ��Һ�õ�ͭ����������õ�FeS��S��
��1�������̿�֪��������ֽ����ɵ�Fe��Cu��Ϊ+2�ۣ�
��2����Ӧ��������ͭ���ӣ�
��3�����Dz�����ܽ�ȣ��ܽ��С���ȴ���Һ��������
��4������ʱΪ�˽��ͺ�̼�����ɽ�����Ͷ�����ڵ������У���������̼��Ӧ��������һ����̼��
��5��������������Ԫ�ػ��ϼ�+4�ۣ�������Ԫ�ص��м��̬�����������Կ������ö�����������ⷴӦ���ɵ���ɫ�������ʣ�NaHSO3��NH4HSO3����ˮ��Һ�������ԣ�������������Һ��������������ӵ���̶ȴ�����ˮ��̶ȣ������������Һ��笠�����ˮ��̶ȴ������������ˮ��̶���Һ�����ԣ�
��6��SO2ͨ��Fe��SO4��3��Һ�У�����������ԭ��Ӧ������������������14H++Cr2O72-+6Fe2+�T2Cr3++6Fe3++7H2O��SO2+2Fe3++2H2O=SO42-+2Fe2++4H+����֪��3SO2��Cr2O72-���Դ˼��㣮
��� �⣺ͭ����S�ڸ��������գ�ʹ��ת��ΪFeS2��CuS������HCl��NaCl��CuCl2�����Һ ������ӦCu2++CuS+4Cl-=2[CuCl2]-+S�������˵õ���Һ��ͨ�����������Ӧ4CuCl2-+O2+4H+=4Cu2++8Cl-+2H2O��һ���¶��£��ڷ�Ӧ�����õ���Һ�м���ϡ���ᣬ������������ͭ���壬�ᾧ����õ�����ͭ���壬��������ԭ��Һ�õ�ͭ����������õ�FeS��S��FeS2ͨ��������յõ��������Ͷ����������������֣����������Ʊ����ᣬ
��1�������̿�֪��������ֽ����ɵ�Fe��Cu��Ϊ+2�ۣ���ӦI�IJ���ΪFeS2��CuS��
�ʴ�Ϊ��FeS2��CuS��
��2����Ӧ��������ͭ���ӣ������ӷ�ӦΪ4CuCl2-+O2+4H+�T4Cu2++8Cl-+2H2O��
�ʴ�Ϊ��4CuCl2-+O2+4H+�T4Cu2++8Cl-+2H2O��
��3����ͬ����������ͭ���ܽ��С������¶��£�����ͭ���ܽ��С���Ȼ�ͭ��������Ӧ�����õ���Һ�м���ϡ���ᣬ������������ͭ���壬
�ʴ�Ϊ�����¶��£�����ͭ���ܽ��С���Ȼ�ͭ���������ᣬ��������������ͭ���壻
��4������ʱΪ�˽��ͺ�̼�����ɽ�����Ͷ�����ڵ������У���������̼��Ӧ��������һ����̼����Ӧ�Ļ�ѧ����ʽΪ��3C+Fe2O3$\frac{\underline{\;����\;}}{\;}$ 2Fe+3CO����
�ʴ�Ϊ��3C+Fe2O3$\frac{\underline{\;����\;}}{\;}$ 2Fe+3CO����
��5��������������Ԫ�ػ��ϼ�+4�ۣ�������Ԫ�ص��м��̬�����������Կ������ö�����������ⷴӦ���ɵ���ɫ�������ʣ���Ӧ�Ļ�ѧ����ʽΪ��SO2+2H2S=3S��+2H2O��NaHSO3��NH4HSO3����ˮ��Һ�������ԣ�������������Һ��������������ӵ���̶ȴ�����ˮ��̶ȣ������������Һ��笠�����ˮ��̶ȴ������������ˮ��̶���Һ�����ԣ���ͬ�����£�ͬŨ�ȵ�����ˮ��Һ��c��SO32-����С����NH4HSO3��
�ʴ�Ϊ��SO2+2H2S=3S��+2H2O�� NH4HSO3��
��6������14H++Cr2O72-+6Fe2+�T2Cr3++6Fe3++7H2O��SO2+2Fe3++2H2O=SO42-+2Fe2++4H+��
��֪��3SO2��Cr2O72-��
3 1
x 0.02mol/L��0.025L
���x=0.0015mol��
��Ӧ������������SO2���������Ϊ��$\frac{0.0015mol}{\frac{0.28L}{22.4L/mol}}$��100%=12.00%��
�ʴ�Ϊ��12.00%��
���� ������ʵ�ʻ�����������ͭ����ۺ����á�Ϊ������������Ԫ�ػ�����֪ʶ�����ӷ���ʽ�ͻ�ѧ����ʽ����д���йؼ��㣬��Ŀ��ע�ؿ���ѧ�����û�ѧԭ�������ʵ����������������ù�ϵʽ����ɼ��㣬��Ŀ�Ѷ��еȣ�


 ��ĩ1�����ʽ���������ϵ�д�
��ĩ1�����ʽ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
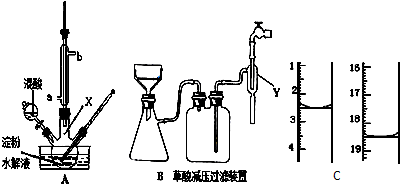
 ��1��ʵ��������ͼ��ʾװ���Ʊ���������������
��1��ʵ��������ͼ��ʾװ���Ʊ���������������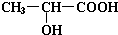 ���Իش�
���Իش�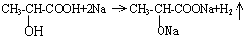 ��
��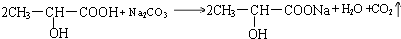 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
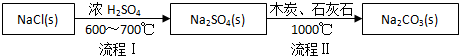
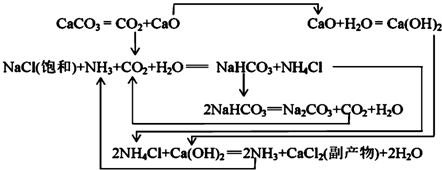
| NaCl | NH4Cl | NaHCO3 | NH4HCO3 | Na2CO3 |
| 35.9 | 37.2 | 9.6 | 21.7 | 21.5 |
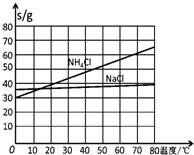
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

| ���� | �۵�/�� | �е�/�� | �ܽ��� |
| �������� | 114.3 | 305 | ������ˮ����������ˮ |
| ���� | -6 | 184.4 | ����ˮ |
| ���� | 16.6 | 118 | ������ˮ |
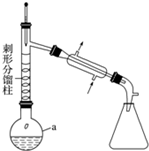
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
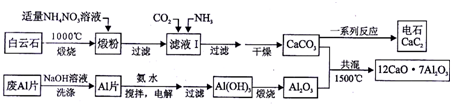
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѧ��Ӧ�е������仯��ͨ������Ϊ�����ı仯 | |
| B�� | ���������������������Ȼ�茶����Ϸų��������÷�ӦΪ���ȷ�Ӧ | |
| C�� | ��Ӧ����1 molˮ������������Ϊ�к��� | |
| D�� | �ɻ�ѧ���������ų������������»�ѧ���γ������յ�����ʱ�������ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 000 mL����ƿ��58.5 g NaCl | B�� | 980 mL����ƿ��57.3 g NaCl | ||
| C�� | 500 mL����ƿ��58.5 gNaCl | D�� | 1 000 mL����ƿ��117.0 g NaC1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com