
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
分析 在元素周期表中,第IA到第VIIA族都是主族元素,包含碱金属族和H元素、碱土金属族、B族、C族、N族、O族、卤族,据此分析解答.
解答 解:在元素周期表中,第IA到第VIIA族都是主族元素,包含碱金属族和H元素、碱土金属族、B族、C族、N族、O族、卤族,这几种元素中,属于主族的是K、O、Si、Mg、Al、Ca、Na,K、Na为第IA族元素,Ca、Mg为第IIA族元素,Al为第IIIA族元素,Si为第IVA族元素,O为第VIA族元素,所以有7种,故选D.
点评 本题考查元素周期表结构及其应用,明确元素在周期表中的位置及周期表结构是解本题关键,熟悉每一主族包含的元素及其性质,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+ Na+NO3- Cl- | B. | K+ Na+Cl- NO3- | ||
| C. | K+ Na+ Cl-AlO2- | D. | K+ NH4+ SO42-NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA | |
| B. | 常温常压下,44 g C3H8中含有的碳碳单键数为3 NA | |
| C. | 6.4 g铜粉与足量硫粉充分反应,失去的电子数为0.2 NA | |
| D. | 1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 固体时能导电的晶体一定为金属晶体 | |
| B. | 电负性差值小于1.7的A、B两种元素,组成的化合物也可能为离子化合物 | |
| C. | 某晶体难溶于水、熔点高、固态不导电,熔化时导电,可判断该晶体为离子晶体 | |
| D. | 由原子构成的晶体均具有熔沸点高、硬度大的特性 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | ($\frac{0.8}{ρ}$)% | B. | ($\frac{0.48}{ρ}$)% | C. | ($\frac{0.32}{ρ}$)% | D. | ($\frac{0.7}{ρ}$)% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 是一种有机烯醚,可以用烃A通过下列路线制得
是一种有机烯醚,可以用烃A通过下列路线制得
| A. | 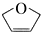 的分子式为C4H4O 的分子式为C4H4O | |
| B. | A的结构简式是CH2=CHCH2CH3 | |
| C. | A能使高锰酸钾酸性溶液褪色 | |
| D. | ①、②、③的反应类型分别为卤代、水解、消去 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com