
某工厂排出的污水中含有大量的Fe2+、Zn2+、Hg2+三种金属离子。以下是某化学研究性学习小组的同
学设计除去污水中的金属离子,并回收绿矾、皓矾(ZnSO4·7H2O)和汞的方案。
【药品】 NaOH溶液、 硫化钠溶液、硫化亚铁、稀硫酸、铁粉
硫化钠溶液、硫化亚铁、稀硫酸、铁粉
【实验方案】
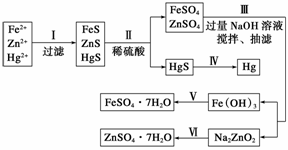
【问题探究】
(1)步骤Ⅱ所发生反应的离子方程式为__________________________________。
(2)步骤Ⅲ中抽滤的目的是____________,该步骤产生Fe(OH)3的反应的离子方程式为
_______________________________________________________________________。
(3)步骤Ⅵ中得到硫酸锌溶液的离子方程式为_________________________________________。
(4)欲实现步骤Ⅴ,需加入的试剂有________、________,所涉及的主要操作依次为_____________。
(5)步骤Ⅳ常用的方法是________,该步骤是否对环境有影响?________(填“是”或“否”),如有影响,请你设计一个绿色环保方案来实现步骤Ⅳ的反应:__________。
(6)该研究小组的同学在强碱溶液中,用次氯酸钠与Fe(OH)3反应获得了高效净水剂Na2FeO4,该反应的离子方程式为___________________________ ____________。
____________。
科目:高中化学 来源: 题型:
把Ba(OH)2溶液滴入到明矾溶液中,使SO42﹣全部转化成BaSO4沉淀,此时铝元素的主要存在形式是()
A. Al3+ B. Al(OH)3 C. AlO2﹣ D. Al3+和Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物其结构简式为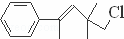 ,关于该有机物下列叙述正确的是()
,关于该有机物下列叙述正确的是()
A. 不能使酸性KMnO4溶液褪色
B. 不能使溴水褪色
C. 在加热和催化剂作用下,最多能和4mol H2反应
D. 一定条件下,能和NaOH醇溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某含Na+的溶液中还可能含有NH4+、Fe3+、Br-、CO32-、I-、SO32-。取样,滴加足量氯水有气泡产生,溶液呈橙色;向橙色溶液中加Ba Cl2溶液或淀粉
Cl2溶液或淀粉
溶液均无现象。为确定该溶液的组成,还需进行的实验有 ( )
A.取样,滴加硫氰化钾溶液
B.取样,加氯水和CCl4,振荡、静置
C.取样,加足量盐酸加热,用湿润的品红试纸检验气体
D.取样,加足量的NaOH浓溶液,加热,用湿润的红色石蕊试纸检验气体
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中评价合理的是 ( )
| 选项 | 化学反应及其离子方程式 | 评价 |
| A | Fe3O4与稀硝酸反应:2Fe3O4+18H+===6Fe3++H2↑+8H2O | 正确 |
| B | 向碳酸镁中加入稀盐酸:CO | 错误,碳酸镁不应写成离子形式 |
| C | 向硫酸铵溶液中加入氢氧化钡溶液: Ba2++SO | 正确 |
| D | FeBr2溶液与等物质的量的Cl2反应: 2Fe2++2Br-+2Cl2===2Fe3++4Cl-+Br2 | 错误,Fe2+与Br-的化学计量数之比应为1∶2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列指定反应的离子方程式正确的是 ( )
A.氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
B.Na2CO3溶液中CO32-的水解:CO32-+H2O=HCO3-+OH-
C.酸性溶液中KIO3与KI反应生成I2:IO3-+I-+6H+=I2+3H2O
D.NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
溶液在25℃时由水电离出氢离子的浓度为1×10﹣12 mol•L﹣1,下列说法正确的是()
A. 该溶液pH=12 B. 该溶液pH=2
C. 该溶液pH=12或2 D. 不能确定溶液pH
查看答案和解析>>
科目:高中化学 来源: 题型:
1988年诺贝尔化学奖授予科恩(美)和波普尔(英),以表彰他们在理论化学领域作出的重大贡献。他们的工作使实验和理论能够共同协力探讨分子体系的性质,引起整个化学领域正在经历一场革命的变化。下列说法正确的是( )
A.化学不再是纯实验化学
B.化学不再需要实验
C.化学不做实验,就什么都不知道
D.未来化学的方向还是经验化学
查看答案和解析>>
科目:高中化学 来源: 题型:
垃圾主要分为生活垃圾、建筑垃圾和工业垃圾三大类。垃圾的危害与处理已成为世界性难题,如一节纽扣电池的有害物质能污染600吨水,一节电池烂在地里,可使一平方米土地失去利用价值。
(1)现在请你根据日常生活中所见到的生活垃圾,设计几种处理垃圾的方法。
__________________________________________________________________
________________________________________________________________。
(2)据报道我国科学家根据干电池各组成的化学性质,采用湿法工艺技术回
收有用物质,废旧电池不仅得到了有效的处理,防止了污染环境,同时又可
回收有用物质,其有关成分可基本全部回收,解决了多年来干电池的回收利
用问题。根据锌锰干电池各组成的化学性质,若用湿法工艺技术回收,可回
收的物质有______________________________________________________。
(3)某城市的一座平房被一起爆炸炸成碎片,经调查这座平房建在一座旧垃
圾堆积场附近。科学家认为引起爆炸的甲烷就来自这一旧垃圾堆积物。回答
下列问题。
① 这一堆积物中包括下列不同物质:玻璃、植物性垃圾、水泥、木屑、钢铁
及塑料。在这些物质中可以产生甲烷气体的是 (至少填两种),写出有关化学方程式 。②如果这一堆积物不被覆盖,而是处于散开状态,那么爆炸可能不会发生,原因是 。③甲烷作为一种绿色能源,在许多家庭安全地使用着,请说明在什么条件下甲烷气体燃烧不安全,并指出不安全因素及排除措施 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com