
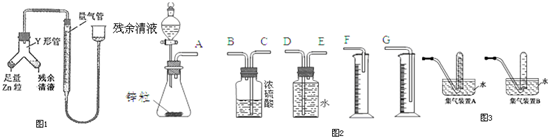
���� ��1�����ݳ������ɵ�BaSO4�����������������ӵ�������û����Һ�������
��2������Һѹ������װ�������ԣ�����װ�ú����������Ҷ�עˮ��ֱ���������߹����γ�һ��Һ��һ��ʱ���Һ���䣻
�ڽ��������Һ���У�Zn����ͭ���ӷ�Ӧ����ͭ���ʣ������������壬ʵ�������DZ�����������ɫ���壬�д������ݣ�п�������ܽ⣻
�۴˷�ӦΪ���ȷ�Ӧ�������������ͣ�δ��ȴ��
��3���ٲ����������������Ͳ�ڵ���Ӧ������Ͳ�ײ�������ѹ���ˮ���ܻ�ճ����Ͳ���ϣ����������������װ��������˳��EDG��
��п�������Һ������ͭ��Ӧ����ͭ��ͭп�γ�ԭ�أ�ʹп�����ᷴӦ���ʼӿ죬��Ӧ���ɴ��������ҷ��ȣ�������ƿ��ѹǿ����
�۸��������֪�����������Ϊ��b-a��mL��1mol����������1mol���������Բ�����Һ����������ʵ���Ϊ$\frac{��b-a����1{0}^{-3}}{22.4}$mol������c=$\frac{n}{V}$�����������ʵ���Ũ�ȣ�
�������ܶȱȿ���С������ˮ���ռ�������Ӧ�̽���
��� �⣺��1��û����Һ�����������������BaCl2��Һֻ�������������ӵ��������������ʣ�������Ũ�ȣ�
�ʴ�Ϊ������������BaCl2��Һֻ�������������ӵ��������������ʣ�������Ũ�ȣ�
��2������Һѹ������װ�������ԣ�����װ�ú����������Ҷ�עˮ��ֱ���������߹����γ�һ��Һ��һ��ʱ���Һ����
�ʴ�Ϊ������װ�ú����������Ҷ�עˮ��ֱ���������߹����γ�һ��Һ��һ��ʱ���Һ���䣻
�ڽ��������Һ���У�Zn����ͭ���ӷ�Ӧ����ͭ���ʣ������������壬ʵ�������DZ�����������ɫ���壬�д������ݣ�п�������ܽ�
�ʴ�Ϊ��Zn����ϡ���������������ɫ���壬�д������ݣ�п�������ܽ⣻
�۴˷�ӦΪ���ȷ�Ӧ�������������ͣ�δ��ȴ��
�ʴ�Ϊ���÷�Ӧ���ȣ�����δ��ȴ��
��3���ٲ�������������������װ��������˳��EDG��
�ʴ�Ϊ��E��D��G��
��п�������Һ������ͭ��Ӧ����ͭ��ͭп�γ�ԭ�أ�ʹп�����ᷴӦ���ʼӿ죬��Ӧ���ɴ��������ҷ��ȣ�������ƿ��ѹǿ����
�ʴ�Ϊ��п�������Һ������ͭ��Ӧ����ͭ��ͭп�γ�ԭ�أ�ʹп�����ᷴӦ���ʼӿ죬��Ӧ���ɴ��������ҷ��ȣ�������ƿ��ѹǿ����
�۸��������֪�����������Ϊ��b-a��mL��1mol����������1mol���������Բ�����Һ����������ʵ���Ϊ$\frac{��b-a����1{0}^{-3}}{22.4}$mol�������ʵ���Ũ��c=$\frac{n}{V}$=$\frac{\frac{��b-a����1{0}^{-3}}{22.4}}{a��1{0}^{-3}}$mol/L=$\frac{b-a}{22.4a}$mol/L��
�ʴ�Ϊ��$\frac{b-a}{22.4a}$mol/L��
�������ܶȱȿ���С������ˮ���ռ�������Ӧ�̽���
�ʴ�Ϊ��B��
���� ���⿼������Ҫ������ͭ��Ũ���ᷴӦ����Һ������Ũ�ȵIJⶨ���漰װ�õķ�����ʵ����������ͻ�ѧ���㣬��Ŀ�Ѷ��еȣ�ע���������ʵ����գ�


 ��ɢ˼ά�¿���ϵ�д�
��ɢ˼ά�¿���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{1}{4}$��$\frac{n��X��}{n��Y��}$��$\frac{3}{2}$ | B�� | $\frac{1}{4}$��$\frac{n��X��}{n��Y��}$��$\frac{1}{2}$ | C�� | $\frac{1}{4}$��$\frac{n��X��}{n��Y��}$��4 | D�� | $\frac{1}{2}$��$\frac{n��X��}{n��Y��}$��4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ijУ��ѧ����С���������ͼʵ��װ�ã����̽��ijЩ���ʵ����ʺͱȽ�����ǿ����ʵ�飮
ijУ��ѧ����С���������ͼʵ��װ�ã����̽��ijЩ���ʵ����ʺͱȽ�����ǿ����ʵ�飮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����ϩ�ĵ���ʽ��
����ϩ�ĵ���ʽ�� ����6.72L����״������ϩ�ͼ���Ļ����ͨ����������ˮ�У���ַ�Ӧ����ˮ������������1.4g��ԭ�����������ϩ�ͼ�������ʵ���֮����1��5
����6.72L����״������ϩ�ͼ���Ļ����ͨ����������ˮ�У���ַ�Ӧ����ˮ������������1.4g��ԭ�����������ϩ�ͼ�������ʵ���֮����1��5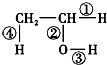 �ڲ�ͬ�Ļ�ѧ��Ӧ�л���Ѳ�ͬ�Ļ�ѧ������д�����з�Ӧ�Ļ�ѧ����ʽ����ָ����Ӧʱ�Ҵ������ж��ѵĻ�ѧ����
�ڲ�ͬ�Ļ�ѧ��Ӧ�л���Ѳ�ͬ�Ļ�ѧ������д�����з�Ӧ�Ļ�ѧ����ʽ����ָ����Ӧʱ�Ҵ������ж��ѵĻ�ѧ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 436kJ | B�� | 557kJ | C�� | 872kJ | D�� | 181kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Һ��һ������Ba2+ | |
| B�� | ����Һ��һ����Na+ | |
| C�� | ��ɫ�����ڱ�״���µ����ԼΪ2.24L | |
| D�� | �������Һ�м�������NaOH��Һ���˳�������ϴ�����պ�����ܵ�8.0g���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ͼ��ʾ����ƿ��ʢ������X���ι���ʢ��Һ��Y������ѹ�ιܽ�ͷ��ʹҺ��Y����ƿ�У�����һ����ɼ�С����a��������X��Һ��Y�������ǣ�������
��ͼ��ʾ����ƿ��ʢ������X���ι���ʢ��Һ��Y������ѹ�ιܽ�ͷ��ʹҺ��Y����ƿ�У�����һ����ɼ�С����a��������X��Һ��Y�������ǣ�������| A�� | X��NH3��Y��ˮ | B�� | X��CO2��Y�DZ���NaHCO3Ũ��Һ | ||
| C�� | X��SO2��Y��NaOH��Һ | D�� | X��HCl��Y��NaNO3ϡ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com