
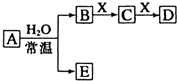
 �ɶ�����Ԫ����ɵ���ѧ��������A��B��C��D��E��X������ͼת����ϵ������������ͷ�Ӧ������ȥ����
�ɶ�����Ԫ����ɵ���ѧ��������A��B��C��D��E��X������ͼת����ϵ������������ͷ�Ӧ������ȥ����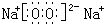 ��X��C��Ӧ����D�����ӷ���ʽΪ��3AlO2-+Al3++6H2O=4Al��OH��3�����ʴ�Ϊ��
��X��C��Ӧ����D�����ӷ���ʽΪ��3AlO2-+Al3++6H2O=4Al��OH��3�����ʴ�Ϊ��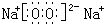 ��3AlO2-+Al3++6H2O=4Al��OH��3����
��3AlO2-+Al3++6H2O=4Al��OH��3����| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ���� | ����Һ��H2SO4����aq�� Ũ�ȣ�mol/L�� | �ζ����ʱ���� ���V��mL�� | ������Һ��NaOH����aq�� ���V��mL�� |
| 1 | 1.000 | 11.00 | 25.00 |
| 2 | 1.000 | 12.04 | 25.00 |
| 3 | 1.000 | 12.18 | 25.00 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2 LҺ̬ˮ�ֽ��2L������1L��������571.6 kJ���� |
| B��2 mol������1mol������Ӧ����2mol��̬ˮ�ų���������571.6 kJ |
| C������ͬ�����£�2 mol������1mol�����������ܺʹ���2molҺ̬ˮ������ |
| D��ʹ�ô����ܽ��÷�Ӧ�Ļ��ʹ��Ӧ�ų�������С��571.6 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����к��Ȳⶨʵ��ʱ����û�л��β�������������û���ͭ�ʽ�������� |
| B���к͵ζ�ʵ���У����ֵ��صζ��ܵĻ��������ֳ���ƿ���۾�ע�ӵζ�����Һ��ı仯 |
| C���������Ͷ����������ֺ���ɫ������õ��۵⻯����Һ������ |
| D����ȥ��������Һ��������NaCl���ɽ�װ�л��Һ�İ�Ĥ����������������ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CO2��SO2����ͨ��ʢ��Ʒ����Һ������ƿ���ռ� |
| B��Fe2+��Fe3+������KSCN��Һ����� |
| C��Cl2��HCl����ͨ��ʢ�б����Ȼ���ˮ��Һ��ϴ��ƿ���ռ� |
| D���Ȼ����Һ��FeCl3����������NaOH��Һ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
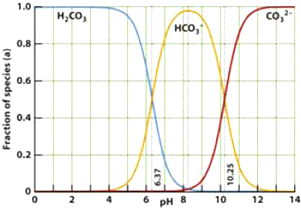
| A����ͼ����ȫ����1.0 mol/L����ζ�1.0 mol/L̼������Һ��ʵ�����ݻ�� |
| B��H2CO3��CO32-����Һ�в��ܴ������� |
| C����1.0 mol/L������뵽�����1.0 mol/L̼������Һ�У���ַ�Ӧ����Һ�ʼ��� |
| D����pHΪ6.37ʱ����Һ�У�c��H2CO3��=c��HCO3-������pHΪ10.25ʱ����Һ�У�c��CO32-��=c��HCO3-�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com